某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分: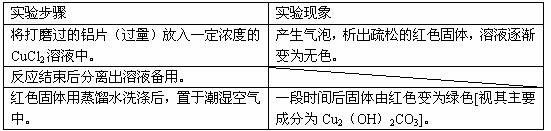
按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)
置换反应____________________________________________________________;
化合反应____________________________________________________________。
(2)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼金属锰。MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+。该反应的离子方程式是 。
(3)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:
①铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于 上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上,不能直接放在桌面上。
实验所用仪器:
a 蒸发皿
b 石棉网
c 泥三角
d 表面皿
e 坩埚钳
f 试管夹
②由粗制氧化铜通过两种途径制取胆矾,通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、 。
据联合国统计,2014年全球电子垃圾数量创历史新高,共达4180万吨,根据预测,到2018年,全球电子垃圾将会增长逾20%,达到5000万吨。将线路板进行处理后,可得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
(1)第①步Cu与混酸反应的离子方程式为______________________________,得到滤渣1的主要成分为_________________,检验滤渣1是否洗涤干净的方法是 。
(2)若滤液1中含有0.5mol Fe2+,则第②步中至少加入H2O2质量为__________________,使用H2O2的优点是_________;调溶液pH的目的是____________________________________。
(3)简述第③步由滤液2得到CuSO4·5H2O的方法是______________________________________ 。
(4)由滤渣2制取Al2(SO4)3·18H2O ,设计了以下三种方案:
上述三种方案中:_______方案不可行,原因是_______________________________;
从原子利用率角度考虑,_______方案更合理。
(5)用滴定法测定CuSO4·5H2O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2+ + H2Y2-→ CuY2-+ 2H+。写出计算CuSO4·5H2O质量分数的表达式ω=_______。
B.【实验化学】塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂。
合成反应原理为:
实验步骤如下:
步骤1在三口烧瓶中放入14.8g邻苯二甲酸酐、25mL正丁醇、4滴浓硫酸,开动搅拌器(反应装置如图)。
步骤2缓缓加热至邻苯二甲酸酐固体消失,升温至沸腾。
步骤3等酯化到一定程度时,升温至150℃
步骤4冷却,倒入分漏斗中,用饱和食盐水和5%碳酸钠洗涤。
步骤5减压蒸馏,收集200~210℃2666Pa馏分,即得DBP产品
(1)搅拌器的作用 。
(2)图中仪器a名称及作用是 ;步骤3中确定有大量酯生成的依据是 。
(3)用饱和食盐水代替水洗涤的好处是 。
(4)碳酸钠溶液洗涤的目的是 。
(5)用减压蒸馏的目的是 。
硅藻土是由硅藻死亡后的遗骸沉积形成的,主要成分是SiO2和有机质,并含有少量的Al2O3、Fe2O3、MgO 等杂质。精制硅藻土因为吸附性强、化学性质稳定等特点被广泛应用。下图是生产精制硅藻土并获得Al(OH)3的工艺流程。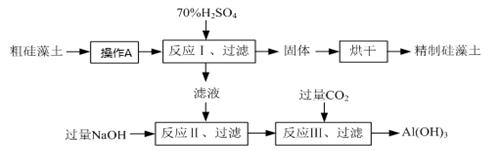
(1)操作A是为了除去粗硅藻土中的有机质,操作A名称为 。
(2)反应Ⅱ中铝元素变化的离子方程式是 ;氢氧化铝常用作阻燃剂,其原因是 。
(3)实验室用酸碱滴定法测定硅藻土中硅含量的步骤如下:
步骤1:准确称取样品a g,加入适量KOH固体,在高温下充分灼烧,冷却,加水溶解。
步骤2:将所得溶液完全转移至塑料烧杯中,加入硝酸至强酸性,得硅酸浊液。
步骤3:向硅酸浊液中加入NH4F溶液、饱和KCl溶液,得K2SiF6沉淀,用塑料漏斗过滤并洗涤。
步骤4:将K2SiF6转移至另一烧杯中,加入一定量蒸馏水,采用70 ℃水浴加热使其充分水解(K2SiF6+3H2O=H2SiO3+4HF+2KF)。
步骤5:向上述水解液中加入数滴酚酞,趁热用浓度为c mol·L-1 NaOH的标准溶液滴定至终点,消耗NaOH标准溶液VmL。
①步骤1中高温灼烧实验所需的仪器除三角架、泥三角、酒精喷灯外还有 (填“瓷坩埚”、“铁坩埚”)。
②实验中使用塑料烧杯和塑料漏斗的原因是 。
③步骤4中水浴加热的目的是 。
④步骤5中滴定终点的现象为 。
⑤样品中SiO2的质量分数可用公式“ ×100%”进行计算。由此分析步骤5中滴定反应的离子方程式为 。
×100%”进行计算。由此分析步骤5中滴定反应的离子方程式为 。
实验室模拟回收某废旧含镍催化剂(主要成分为NiO,另含Fe2O3、CuO、BaO等)生产Ni2O3。其工艺流程为:
(1)浸出渣主要成分的化学式为 。镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是 。
(2)操作A得到的溶液中铁元素的存在形式为 (写化学式),该反应生成硫单质的化学方程式 。
(3)操作B中是为了除去滤液中的铁元素,写出操作步骤: 。
(4)电解产生2NiOOH·H2O的原理分两步:①碱性条件下Cl-在阳极被氧化为ClO-;②Ni2+被ClO-氧化产生2NiOOH·H2O沉淀。第②步反应的离子方程式为 。
已知镁能在二氧化碳中燃烧,反应的化学方程式为2Mg+CO2 2MgO+C。某课外活动小组根据Mg与CO2的反应原理,探究Mg与SO2的反应及固体产物,实验装置如图所示。请回答下列问题:
2MgO+C。某课外活动小组根据Mg与CO2的反应原理,探究Mg与SO2的反应及固体产物,实验装置如图所示。请回答下列问题:
(1)装置A中发生反应的化学方程式为______________。
(2)装置B中盛装的干燥剂可以是_______(填序号)。
①浓硫酸②无水CaCl2③碱石灰④五氧化二磷
(3)实验开始时,先让A中反应进行一段时间,然后再点燃C处酒精灯,这样做的目的是_______。
(4)D装置的作用是___________,发生反应的离子方程式为______________________。
(5)甲同学认为镁与SO2反应的方程式应该是2Mg+SO2 2MgO+S;
2MgO+S;
乙同学认为硫是活泼的非金属,发生的反应应该是3Mg+SO2 2MgO+MgS;
2MgO+MgS;
而丙同学认为SO2是酸性氧化物,发生的反应应该是:2Mg+3SO2 2MgSO3+S。
2MgSO3+S。
要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
已知:MgSO3和MgS都是微溶于水,且都能与盐酸发生复分解反应放出气体;
限选试剂:2mol/L HCl、2mol/L HNO3、蒸馏水、2mol/LNaOH、品红溶液、澄清石灰水、2mol/LCuSO4;仪器和用品自选。请填写下表中的空格:
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量反应后所得固体样品于试管Ⅰ中 |
|
| 步骤2:向试管Ⅰ中的固体慢慢滴加__________, 试管Ⅰ口塞上带导管的单孔塞,并将导管插入盛有________的试管Ⅱ中。 |
a.若试管Ⅰ中的固体未完全溶解,且_______,则甲同学的推测是正确的。 b.若试管Ⅰ中的____________,则乙同学的推测正确。 |
根据上述实验探究,能证明丙同学推测正确的操作和预期现象是_________________。