小华同学想制取“叶脉书签”,需要50 g质量分数为10%的氢氧化钠溶液。请回答下列问题:
(1)若用氢氧化钠固体配制,需称取氢氧化钠 g。
(2)若用25%的氢氧化钠溶液配制,需25%的氢氧化钠溶液 g;量取配制时所用的蒸馏水应选 mL(选填“10”、“20”、“50”、“100”)的量筒(水的密度为1 g/cm3)。
(3)下列操作正确的是 (填字母)。
| A.在托盘天平的左右托盘上垫质量相同的滤纸直接称取氢氧化钠固体 |
| B.将准确称取的氢氧化钠固体直接倒入装有水的量筒中溶解 |
| C.将配制好的氢氧化钠溶液装入广口瓶中,塞好橡胶塞并贴上标签 |
| D.为了加快氢氧化钠的溶解速率,溶解过程中用玻璃棒不断搅拌 |
请从铜、锌、钛、铁、钙、银、铝、汞、钨等金属中选取合适的答案填入下面空格中:
(1)用于干电池的是;
(2)广泛应用于电视、微机中作导体的是;
(3)广泛用于航空、航天及化学工业的是;
(4)铁栏杆外层涂料的“银粉”大多是;
(5)体温计中银白色的液体是;
(6)热水瓶内胆壁常镀一层银白色物质中有;
(7)世界年产量最高的金属是。
我市某化工厂排放的尾气中除含CO2外,还可能含有CO等气体。为确认CO气体是否存在,实验小组利用下列装置进行了检验,请回答下列问题: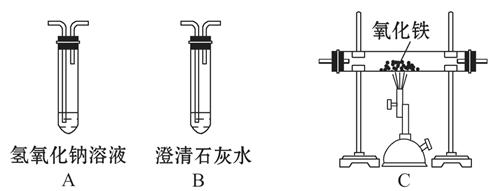
(1)在实验时,上述装置的连接顺序是:A→B→C→B。其中A装置的作用是,第一次B装置的作用为。
(2)若CO气体存在,则装置C中实验现象为,反应的化学方程式为。
(3)从环境保护的角度考虑,你认为该实验的设计应如何改进?请写出一种改进方法:。
金属材料在生活、生产中应用十分广泛。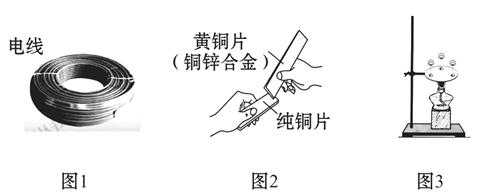
(1)图1是金属的一个应用实例,请说出利用了金属的什么物理性质?。(答出一点即可)
(2)图2中两块金属片互相刻划后,在纯铜片上有明显的划痕。该实验探究的目的是。
(3)将绿豆粒大小的金属焊锡、锡和铅放置在铁片上(呈三角形摆放),加热铁片的中心部分(使三种金属材料温度同步上升),可以观察到焊锡稍加热即熔化,继续加热锡熔化,铅最后熔化。该实验结论是。
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:
请问:①操作Ⅰ的名称是。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和;
②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将。(填“偏大”“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为g。(用a、b、c表示)
由我国化工专家侯德榜探索发明的“侯氏制碱法”,其生产过程涉及的主要化学反应如下:
①NH3+CO2+X=NH4HCO3
②NH4HCO3+NaCl=NH4Cl+NaHCO3↓
③2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
请回答:(1)反应①中X的化学式为;
(2)NH4Cl中氮元素的化合价为;
(3)除去混在Na2CO3粉末中少量的NaHCO3的方法是。