人类的日常生活和工农业生产离不开水。
(1)取2个烧杯,各盛大半烧杯浑浊的天然水,向其中1个烧杯中加入3药匙明矾粉末,搅拌溶解后,静置一段时间,观察到的现象是 。
(2)如图所示,在电解器玻璃管内加满水,接通直流电源,一段时间后切断电源,用燃着的木条分别在两个玻璃管尖嘴口检验电解反应中产生的气体。完成下表:
| |
气体体积 |
用燃着的木条检验气体时的现象 |
| 正极端玻璃管 |
mL |
|
| 负极端玻璃管 |
10mL |
|
(3)工业上可以利用甲烷与水蒸气在一定条件下发生反应来制取氢气,化学方程式为CH4+H2O一定条件CO+3H2。若用该方法制取150kg氢气,消耗甲烷的质量是多少?(写出计算过程)
鸡蛋壳的主要成分是碳酸钙(其他成分不与水也不与盐酸反应)。为了测定鸡蛋壳碳酸钙的含量,进行如下实验:
请回答下列问题:
(1)鸡蛋含有的营养素主要为。
(2)计算鸡蛋壳中碳酸钙的质量分数(写出简明的计算过程)。
一瓶未贴标签的粉末状常见金属
。为了测定
的相对原子质量,准确称取一定量金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重。重复实验,获得如表数据。请回答:
| 实验次数 |
金属质量(
) |
金属氧化物质量(
) |
| l |
45.0 |
84.9 |
| 2 |
45.0 |
85.1 |
| 3 |
45.0 |
85.O |
| 平均值 |
45.0 |
(1)表格中
。
(2)该金属氧化物中,
元素和氧元素的质量比为。
(3)已知
的化合价为+3价,则
的相对原予质量为。
黄铁矿矿石的主要成分为二硫化亚铁(
),取一块质量为30克的黄铁矿矿石样品在氧气中完全灼烧后得到10克氧化铁(其中的铁全来自二硫化亚铁)同时生成二氧化硫。
(1)二硫化亚铁中硫元素的化合价为
(2)计算黄铁矿矿石样品中二硫化亚铁的质量分数。
把萝卜块放入浓盐水中,萝卜块会皱缩。把姜焉的青菜放入清水中,青菜会变挺。这就都是生话常识,其中蕴含着科学道理,启迪我们去思考。
(1)观察人体口腔上皮细胞时,为什么要将口腔上皮细胞除抹在生理盐水(溶质质量分数为0.9%的氯化钠溶液)中?
(2)现有100克溶质质量分数为4.5%的氯化钠溶液,将它稀释成溶质质量分数为0.9%的生理盐水,需加水多少毫升?
学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名"愚人金"),为进一步定量分析黄铜的成分,某同学进行了如下实验:称量黄铜样品
放入锥形瓶中,向其中不断加入稀硫酸,收集生产的气体与所加稀硫酸的质量关系如图所示。求: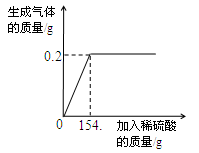
(1)黄铜样品中锌的质量
(2)恰好完全反应时,所得溶液中溶质的质量分数。