在一定条件下,有可逆反应 。当单独改变下列条件后,有关叙述中错误的是
。当单独改变下列条件后,有关叙述中错误的是
A.加入氩气,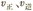 都增大,且 都增大,且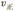 增大倍数大于 增大倍数大于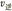 增大倍数 增大倍数 |
B.加入催化剂,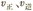 都发生变化,且变化的倍数相同 都发生变化,且变化的倍数相同 |
C.增大压强时,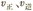 都增大,且 都增大,且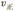 增大倍数大于 增大倍数大于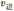 增大倍数 增大倍数 |
D.降低温度时,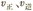 都减小,且 都减小,且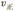 减小倍数小于 减小倍数小于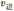 减小倍数 减小倍数 |
下列离子方程式与所述事实相符且正确的是
| A.苯酚钠溶液中通入少量CO2: CO2 + H2O + 2C6H5O-→ 2C6H5OH + CO32- |
| B.向氯化亚铁溶液中通入氯气:Fe2+ + Cl2 ="=" Fe3+ + 2Cl- |
C.用惰性电极电解饱和NaCl溶液:2Cl-+ 2H+  H2↑+ Cl2↑ H2↑+ Cl2↑ |
| D.Na2SO3溶液使酸性KMnO4溶液褪色: |
5SO32-+ 6H+ + 2MnO4-==5SO42-+ 2Mn2+ + 3H2O
下列与实验相关的叙述正确的是
| A.从碘水中提取单质碘时,可用无水乙醇代替CCl4 |
| B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 |
| C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏高 |
| D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
下列液体均处于25℃,有关叙述正确的是
| A.Na2CO3溶液中,c(OH-)-c(H+)=c(HCO3-) +2c(H2CO3) |
| B.AgCl在同浓度的MgCl2和KCl溶液中的溶解度相同 |
| C.将稀氨水逐滴加入稀硫酸中,当溶液pH = 7时,c(SO42-) > c(NH4+) |
| D.Na2S溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
化学与生活密切相关,下列有关说法正确的是
| A.富含蛋白质的食物多属于碱性食物 |
| B.青霉素具有消炎作用,使用前要进行皮肤敏感试验 |
| C.石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
| D.使用太阳能热水器、沼气的利用、玉米制乙醇都涉及生物质能的利用 |
下列做法不能体现低碳生活的是
| A.减少食物加工过程 | B.注意节约用电 |
| C.大量使用薪柴为燃料 | D.尽量购买本地的当季的食物 |