X、Y为同主族元素,Y的原子半径大于X。下列说法正确的是(m、n均为正整数)
| A.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| B.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| C.若HnY的水溶液为酸性,则HnX的酸性比HnY的酸性更强 |
| D.若Y的最高正价为+7,则X的最高正价一定为+7 |
下列有关钠的物理性质的叙述中正确的是
①银白色金属;②质软,可以用小刀切割;③熔点低于100 ℃;④密度比水小;⑤热和电的良导体
| A.①②④ | B.①②③④ | C.①③④ | D.①②③④⑤ |
下列物质中,不属于合金的是
| A.硬铝 | B.黄铜 | C.钢铁 | D.水银 |
考古学上常用碳元素的一种核素 来测定文物的历史年代。下列关于
来测定文物的历史年代。下列关于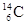 的叙述中,错误的是
的叙述中,错误的是
| A.质子数是6 | B.核外电子数是6 | C.中子数是6 | D.质量数是14 |
下列物质中,属于离子化合物的是
| A.HNO3 | B.H2O2 | C.C2H4 | D.NH4Cl |
若在试管中加入2-3 mL液体再加热,正确的操作顺序是
①点燃酒精灯进行加热;②在试管中加入2-3 mL液体;③用试管夹夹持在试管的中上部;④将试剂瓶的瓶盖盖好,放在原处。
| A.②③④① | B.③②④① | C.②④③① | D.③②①④ |