“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是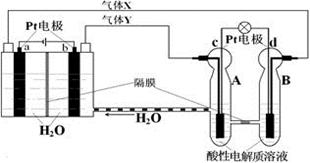
A.转移0.1mol电子时,a电极产生1.12LH2
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-===LiFePO4负极 Li-e-===Li+,下列说法中正确的是
| A.充电时电池反应为FePO4+Li ="==" LiFePO4 |
| B.充电时动力电池上标注“+”的电极应与外接电源的正极相连 |
| C.放电时,在正极上是Li+得电子被还原 |
| D.放电时电池内部Li+ 向负极移动 |
下列装置或操作的叙述中错误的是
| A.①可以用于利用铜与盐酸反应制取氯化铜溶液 |
| B.②可以用于比较碳酸钠与碳酸氢钠的热稳定性 |
| C.③可以从海水中提取淡水 |
| D.④可以用于稀释浓硫酸 |
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
(1)4FeO·Cr2O3+8Na2CO3+7O2高温8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是
| A.反应(1)和(2)均为氧化还原反应 |
| B.反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3 |
| C.Na2Cr2O7中Cr元素的化合价为+7 |
| D.反应(1)中生成1mol的Na2CrO4时共转移28mol电子 |
铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅等,工业上经过下列工艺可以冶炼金属铝。下列说法错误的是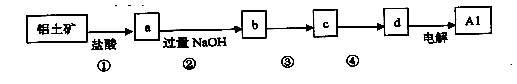
| A.①、②中除加试剂外,还需要进行过滤操作 | B.a、b中铝元素的化合价相同 |
| C.③中需要通入过量的氨气 | D.④进行的操作是加热,而且d一定是氧化铝 |
下列关于有机物的说法正确的是
| A.苯、乙酸和油脂都可以发生取代反应 |
| B.石油经过分馏得到的汽油、煤油等馏分都是纯净物 |
| C.乙烯、聚乙烯都能使酸性高锰酸钾溶液褪色 |
| D.在一定条件下,葡萄糖、淀粉、蛋白质都可发生水解反应 |