下列示意图与对应的反应情况正确的是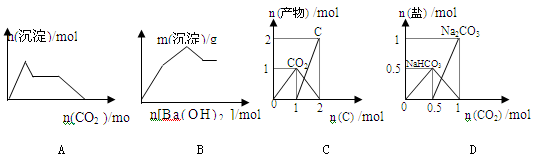
| A.含0.01molKOH 和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| C.n(O2)=1mol时,高温下C和O2在密闭容器中的反应产物 |
| D.n(NaOH)=1mol时,CO2和NaOH溶液反应生成的盐 |
地壳中含量最多的金属元素和含量最多的非金属元素所形成的化合物是
| A.Fe3O4 | B.Al2O3 | C.SiO2 | D.CuO |
下列区别物质的方法错误的是
| A.铝与铝合金—比较硬度 | B.用水区别氯化钠和硝酸铵固体 |
| C.用燃烧的方法区别羊毛和涤纶 | D.用燃着的木条鉴别氮气与二氧化碳 |
下列实验操作正确的是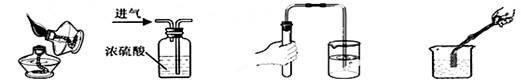
| A.点燃酒精灯 | B.干燥氢气 | C.检查气密性 | D.测定溶液的pH |
“无土栽培”是一项利用化学试剂配成的营养液来栽培植物的新技术.下列是某营养液所含的主要成分,其中属于复合肥料的是
| A.KNO3 | B.CO(NH2)2 | C.Ca(H2PO4)2 | D.(NH4)2SO4 |
依据国家相关法律规定,机动车驾驶员醉驾将受到刑事处罚。检测驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器。在K2Cr2O7中Cr元素的化合价是
| A.+2 | B.+3 | C.+6 | D.+7 |