现有下列几种物质:
①CaS ②Ar ③CaO2 ④金刚石 ⑤SiC ⑥H2O2 ⑦(NH4)2SO4 ⑧MgCl2 ⑨CH3COONa ⑩[Cu(NH3)4]SO4 (以下空格均填写序号)
(1)不含极性键的分子晶体是 ;(2)含有极性键的分子晶体是 ;
(3)只含离子键的离子晶体是 ;(4)含有极性键的原子晶体是 ;
(5)含有非极性键的离子晶体是 ;(6)含有配位键的离子晶体是 。
X、Y、Z、W、Q均为短周期元素,原子序数依次增大,X、Q同主族,X元素的原子半径最小,Y元素原子的最外层电子数是内层电子数的2倍,Z元素的最高价氧化物的水化物甲与其气态氢化物化合生成一种盐乙;X、Y、Z、Q四种元素都能与W元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)Q的原子结构示意图为。
(2)Y和W相比,非金属性较强的是(用元素符号表示),下列事实能证明这一结论的是____(选填字母序号)。
a.常温下,Y的单质呈固态,W的单质呈气态
b.W的气态氢化物的稳定性强于Y的气态氢化物
c.Y与W形成的化合物中,Y呈正价
d.W的最高价氧化物的水化物酸性强于Y的最高价氧化物的水化物
(3)X、Y、W、Q四种元素组成的某无机化合物,受热易分解。写出少量该化合物的溶液与足量的Ca(OH)2溶液反应的离子方程式:。
(4)常温下,甲、乙的水溶液pH均为5。则甲、乙的水溶液中由水电离出的H+浓度大小关系为:甲____乙(填“>”、“<”或“=”)。
(5)利用原电池原理,将X、Z的单质气体分别通人电池的两极,用质子导电陶瓷传递H+,可合成ZX3,该电池的正极反应式为。
A、B、C、D、E是中学常见的五种化合物,A、B是氧化物,X、Y是生活中常见的金属,相关物质间的关系如下图所示(某些条件已略去)。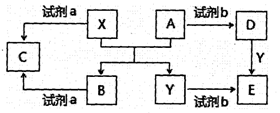
(1)若试剂a是NaOH溶液。
①C的名称是____。
②B与试剂a反应的离子方程式是。
(2)若试剂b是稀H2SO4。
①D的化学式是。
②某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应化学方程式是:。

(1)①用1.0 mol·L-1盐酸配制100 mL 0.10 mol·L-1盐酸,所需的玻璃仪器有量筒、
100 mL容量瓶、烧杯、、。
②用0.10 mol·L-1标准盐酸滴定未知浓度的烧碱溶液时,酸式滴定管初读教为0.10
mL,终读数如右图所示,则滴定所用盐酸体积为____。
(2)如右图所示,集气瓶内充满某混合气体,置于光亮处一段时间,
将滴管内的水挤入集气瓶,再打开止水夹,烧杯中的水会进入
集气瓶。该集气瓶中的气体可能是。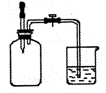
| A.CO、O2 |
| B.Cl2、CH4 |
| C.NO2、O2 |
| D.N2、H2 |
某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。向乙中滴入酚酞试液,将电源接通后,在F极附近显红色。试回答下列问题:
(1)电源A 极的名称是___________。
(2)甲装置中电解反应的 总化学方程式是
总化学方程式是
______________________________。
(3)如果收集乙装置中产生的气体,两种气体的体积比是_________ _。
_。
(4)欲用丙装置给铜镀银,G应该是______(填“铜”或“银”),电镀液是_______(填化
学式)溶液。
(5)装置丁中的现象是________________________________________。
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。
A. KMnO4 B. H2O2 C. Cl2水 D. HNO3
然后再加入适当物质调整至溶液pH=3.8,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损
失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=3.8是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可
以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,
Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1
时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的
pH为________ ,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填
,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填
“可行”或“不可行”)。