恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)="13" mol,n (NH3)="6" mol, a="________" 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。n(NH3) __________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)= _____ 。
(4)原混合气体中,a:b= 。
(5)将1molN2和3molH2合成NH3反应时,下列叙述能说明该反应已达到化学平衡状态的是(填标号)_________ ;
| A.容器内的总压强不随时间而变化 |
| B.反应后混合气体的密度不再发生变化 |
| C.三种气体的浓度相等且保持不变 |
| D.NH3的分解速率与生成速率相等 |
E、混合气体的平均相对分子质量不再发生变化
用稀盐酸和氢氧化钡溶液进行酸碱中和反应实验,该反应过程中溶液酸碱度变化及相关数据如右图所示。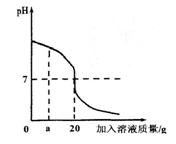
(1)根据此变化曲线,你认为实验操作是将滴加到另一种溶液中。
(2)当加入溶液质量是a g时,溶液中溶质是(写化学式)。
(3)若用pH试纸测定溶液的酸碱度,请写出测定方法:。
(4)当pH=7时,测得生成氯化钡的物质的量为0.05mol,求盐酸中溶质的质量分数?
右图中两圆相交部分(A、B、C、D)可表示铁、稀硫酸、烧碱溶液、硫酸铜溶液间的反应关系,请按下列要求填空:
(1)A处产生的现象是
(2)B处发生反应的类型是;
(3)C处发生反应的化学方程式是 ;
(4)D处发生反应的化学方程式是 。
23.75g某+2价金属氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量_______________MCl2的相对分子质量为_________,M的相对原子质量为_________。
(1)1.5molH2SO4的质量是______g,其中含有_____mol H,含有_______g氧元素。
(2)9.03×1023个氨(NH3)分子含___________mol氨分子,____________mol氢原子,________mol质子,________________个电子。
(3)硫酸铝的化学式为___________,0.2mol硫酸铝中有______molAl3+,__个SO42-。
(4)0.5mol H2O与_________g硫酸所含的分子数相等,它们所含氧原子数之比是_________,其中氢原子数之比是_________。
下列物质中① CO2② HNO3③KOH ④石墨⑤ Fe ⑥葡萄糖⑦Na2CO3⑧酒精⑨食盐水
(1)属于电解质的是_____________________________
(2)属于非电解质的是___________________________
(3)写出电解质的电离方程式