氢化钠(NaH)是一种白色晶体,NaH与水反应放出H2,下列叙述正确的是
| A.NaH在水中显酸性 | B.NaH中氢离子电子层排布与氦相同 |
| C.NaH中氢离子半径比锂离子半径小 | D.NaH中氢离子被还原为H2 |
某矿石由前20号元素中的4种组成,其化学式为WYZX4。X、Y、Z、W分布在三个周期,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体。下列说法正确的是()
| A.原子半径:W>Y>Z>X | B.气态氢化物的稳定性:X <Z |
| C.最高价氧化物对应水化物的碱性:Y>W | D.Y、Z的氧化物都有两 性 性 |
已知下列反应的热化学方程式为:C(s)+O2(g)=CO2(g)△H1=—393.5kJ/niol
CH3COOH(1)+2O2(g)= 2CO2(g)+ 2H2O(1)△H2="-" 870.3kJ/mol
H2(g)+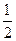 O2(g)=H2O(1)△H="-285.8" kJ/mol
O2(g)=H2O(1)△H="-285.8" kJ/mol
则2C(s)+2H2(g)+O2(g)=CH2COOH(1)的反应热△H为
| A.+488.3kJ/mol | B.-488.3kJ/mol |
| C.-244.15kJ/mol | D.+244.15kJ/mol |
NA表示阿伏加德罗常数的值,下列判断正确的是()
| A.lmol Cu在适量硫蒸气中燃烧,得到的固体质量为80g |
| B.分子数为NA的CO、C2H4的混合气体体积约为22.4L,质量为28g |
| C.56g Fe投入足量冷的浓硝酸中,转移的电子数为3NA |
D.0.lmol1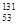 I愿子中含电子数为7.8NA I愿子中含电子数为7.8NA |
分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应。在一定条件下与H2完全加成,加成后其一氯代物的同分异构体(不考虑立体结构)有()
| A.3种 | B.4种 | C.5种 | D.6种 |
下列有关叙述中错误的是
| A.纤维素分子是由葡萄糖单元构成的,可以表现出一些多元醇的性质 |
| B.蔗糖和淀粉的水解产物不同 |
| C.判断油脂皂化反应基本完成的现象是反应后静置,反应液不分层 |
| D.煤中含有苯和甲苯,可用先干馏后分馏的方法得到 |