在t℃时,10L 0.4mol·L-1H2O2溶液发生催化分解:2H2O2 = 2H2O + O2↑,不同时刻测得生成O2的体积如下表,已知反应至6min时,H2O2分解了50%(已折算为标准状况)
| t /min |
0 |
2 |
4 |
6 |
| V(O2)/L |
0.0 |
9.9 |
17.2 |
V=? |
下列叙述正确的是(溶液体积变化忽略不计)
A.0~2min H2O2平均反应速率比4~6min慢
B.反应至6min时,共产生O2 44.8L
C.0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol·L-1·min-1
D.反应至6min时,c(H2O2) = 0.3mol·L-1
2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是
| A.单质钠的密度比钾的密度小 |
| B.钠和钾在空气中燃烧的产物都是过氧化物 |
| C.钠和钾都是短周期元素 |
| D.钠和钾的合金[ω(K)=50%-80%]在室温下呈液态 |
在海洋底部存在大量的称为“可燃冰”的物质,其蕴藏量是地球上煤石油的百倍,因而是一种等待开发的巨大能源。初步查明可燃冰是甲烷、乙烷等可燃气体跟水的结合产物。有关可燃冰的下列推测中错误的是
| A.高压、低温有助于可燃冰的形成 |
| B.常温常压下,可燃冰是一种稳定物质 |
| C.可燃冰的微粒间可能存在氢键 |
| D.构成可燃冰的原子间存在极性共价键 |
下列有机物有四种同分异构体的是()
| A.分子式为C4H10的二氯取代物 |
| B.分子式为C4H8O2的有机物 |
| C.乙苯的一氯取代物 |
| D.分子式为C3H9N的有机物,其中N原子以三个单键与其他原子相连 |
今有室温下四种溶液,有关叙述不正确的是()
| ① |
② |
③ |
④ |
|
| pH |
11 |
11 |
3 |
3 |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A、分别加水稀释10倍,四种溶液的PH①>②>④>③
B、①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
C、①、④两溶液等体积混合,所得溶液中c(Cl—)>c(NH4+)>c(OH—)>c(H+)
D、Va L④与VbL②溶液混合后,若混合后溶液PH = 4,则Va : Vb =" 11" : 9
对于可逆反应 A(g) +2B(g)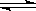 2C(g)△H>0,下列图像中正确的是()
2C(g)△H>0,下列图像中正确的是()