某学习小组依据SO2性质,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是_________________________________。
Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和______________________的洗气瓶。
Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,充分反应后,将液体和剩余气体分离,进行如下研究。
(1)向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
①写出SO2Cl2与H2O反应的化学方程式____________________________ 。
②检验该溶液中Cl-的方法是___________________________________________________。
(2)用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。该白色沉淀的成分是___________________________。
滴定实验是化学学科中重要的定量实验。 请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是______(填选项字母)
A、滴定终点读数时,俯视滴定管刻度,其他操作正确。
B、盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C、酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D、滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
| 滴定次数 |
待测液体积(mL) |
标准KMnO4溶液体积(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
3.00 |
23.00 |
| 第三次 |
25.00 |
4.00 |
24.10 |
①滴定时,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是 。
②该草酸溶液的物质的量浓度为_____________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
| 难溶物 |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
| 颜色 |
白 |
浅黄 |
白 |
砖红 |
白 |
| Ksp |
1.77×10-10 |
5.35×10-13 |
1.21×10-16 |
1.12×10-12 |
1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
实验室要用Na2CO3·10H2O晶体配制500 mL 0.1 mol·L-1 Na2CO3溶液,回答下列问题:
(1)应该用托盘天平称取Na2CO3·10H2O________g。
(2)如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是________mL。
(3)若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.定容前容量瓶底部有水珠______________________________________;
B.定容时加水超过刻度线________________________________________;
C.最终定容时俯视观察液面 。
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 |
Na+、K+、Cu2+ |
| 阴离子 |
SO42-、OH- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加了8 g。常温下各烧杯中溶液的pH与电解时间t的关系图如下。据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”)。
(2)计算电极e上生成的气体在标准状况下的体积为_________________。
(3)B溶液中的溶质为 。电解后,乙烧杯中溶液的pH=__________。 若在B溶液中事先滴加紫色石蕊试液, 极(填写“c”或“d”)先变红。
某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题: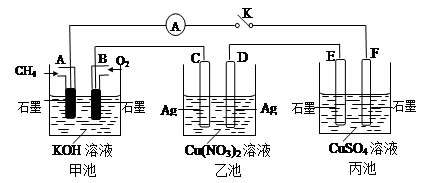
(1)甲池A电极的电极反应式为 。
(2)丙池中电解反应的方程式是 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
用质量分数为98%密度为1.84g·cm-3的浓硫酸配制250mL物质的量浓度为2mol·L-1的稀硫酸。其操作步骤可分解为以下几步:
A.用量筒量取 mL浓硫酸, (简述浓硫酸稀释的操作),冷却
B.检查 (填所用仪器名称)是否漏水
C.用蒸馏水洗涤烧杯和玻璃棒2~3次,将每次的洗涤液都转移入容量瓶里
D.将稀释后的硫酸小心地用玻璃棒引流至容量瓶里
E.盖紧瓶塞,上下倒转摇匀溶液
F.将蒸馏水直接加入容量瓶至刻度线以下2cm处
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到凹液面最低点恰好与刻度线相切
请据此填写:
(1)完成上述步骤中的空白处。
(2)正确的操作顺序是(用字母填写):()→()→()→()→()→()→()
(3)进行A步操作时,选用量筒的规格是 。(选填字母)
A.10mL B.50mL C.100mL D.1000mL
(4)下列情况对所配制的稀硫酸浓度有何影响?(选填“偏高”、“偏低”、“无影响”)。
①.用量筒量取浓硫酸时俯视,则 ;
②.A 步操作时,浓硫酸稀释后,未冷却即进行下一步操作,则_________;
③.定容时仰视溶液的凹液面,则_________。