已知可逆反应:N2(g)+3H2(g)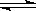 2NH3(g) △H=-92kJ·mol-1下列关于此反应的说法中错误的是
2NH3(g) △H=-92kJ·mol-1下列关于此反应的说法中错误的是
| A.压缩反应容器使气体体积减小,可使该反应的反应速率变大 |
| B.该反应中反应物的总能量比生成物的总能量高 |
| C.单位时间内生成1molN2,同时消耗3molH2,说明该反应达到平衡状态 |
| D.将1molN2和3molH2混合进行反应,共放出的热量为92kJ |
下列大小顺序排列不正确的组合是
| A.气态氢化物的稳定性:H2O > H2S >SiH4 | B.离子半径:Cl-> O2-> Mg2+ |
| C.物质酸性: H3PO4 > H2SO4 > HClO4 | D.熔点:KCl > KI > K |
在下图所示装置中,将溶液A逐滴加入固体B中,下列叙述中不正确的是
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色 |
| B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 |
| C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀 |
| D.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色 |
设NA代表阿佛加德罗常数,下列说法中正确的是
①常温常压下,1 mol氦气含有的核外电子数为4NA
②常温常压下,17 g甲基(—14CH3)所含的中子数为8NA
③0.44 g C3H8中含有的共用电子对总数目为0.08NA
④常温常压下,100 mL 0.5 mol/L 的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标准状况下,22.4 L SO3中含有的氧原子数为3NA
⑥常温常压22.4 L NO气体的分子数小于NA
| A.①②⑤ | B.③④⑤ | C.②④⑥ | D.③⑤⑥ |
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.pH=13的溶液:Na+、K+、SiO32-、HSO3- |
| B.含较多的SO32-的溶液:H+、NH4+、Fe3+、Cl- |
| C.澄清透明溶液中:K+、Na+、MnO4-、SO42- |
| D.滴入甲基橙显红色的溶液中:NH4+、Ba2+、Al3+、ClO- |
在火箭升空过程中,主要以偏二甲肼CH3-NH-NH-CH3(其中N可看做—1价)为燃料,发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O提供能量。下列叙述正确的是
| A.该反应涉及的物质均绿色环保,在燃烧过程中不会造成任何环境污染 |
| B.该反应的三种产物均含有非极性键 |
| C.此反应中氧化产物和还原产物的物质的量之比为2:3 |
| D.每有0.6 mol N2生成,转移电子数目为3.2NA |