现有如下各说法:
①在水分子中氢、氧原子间以共价键相结合
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl = H+ + Cl-,判断HCl分子里存在离子键;
⑤冰的密度比水的密度小,这与氢键有关
上述各种说法正确的是
| A.①②⑤ | B.①②④⑤ | C.①②③④⑤ | D.①③④⑤ |
下列关于合成材料的说法中,不正确的是………………………………………()
| A.塑料、合成纤维和合成橡胶都属于合成材料 |
| B.聚氯乙烯可制成薄膜、软管等,其单体是CH2 = CHCl |
| C.合成酚醛树脂的单体是苯酚和甲醇 |
D.合成顺丁橡胶(  )的单体是CH2=CH—CH=CH2 )的单体是CH2=CH—CH=CH2 |
在通常条件下,下列各组物质的性质排列正确的是…………………………… ()
| A.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | B.水溶性: HCl>H2S> SO2 |
| C.还原性:HF>HCl>HBr>HI | D.热稳定性:HF>H2O>NH3 |
X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示。
| 元素 |
部分结构知识 |
部分性质 |
| X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氢化物 |
| Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
| W |
W原子的最外层电子数等于2n-3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
1、X单质分子的结构式是 ,Z元素原子最外层共有_____种不同运动状态的电子。
2、X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是 。
3、常温时,W的硫酸盐溶液的pH7(填“=”、“>”或“<”),理由是:
(用离子方程式表示)。
4、25℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6 kJ的热量,写出该反应的热化学方程式 。
下列化学用语或图示表达正确的是…………………………………………( )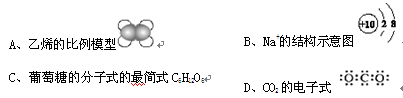
PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也叫可入肺颗粒物,与肺癌、哮喘等疾病的发生密切相关,是灰霾天气的主要原因,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等,下列与PM 2.5相关的说法不正确的是…………………( )
| A.大力发展电动车,减少燃油汽车的尾气排放量 |
| B.开发利用各种新能源,减少对化石燃料的依赖 |
| C.多环芳烃是强致癌物,能吸附在PM 2.5的表面进入人体 |
| D.PM 2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |