化学兴趣小组用如图所示装置探究炼铁的原理.
(1)加热Fe2O3之前要先通一会儿CO,目的是________.
(2)方框中连接的是C和D,导管接口的连接顺序为a→( )→( )→( ),如果导管连接错误,后果是________________.(提示:CO既不溶于水也不与NaOH溶液反应,CO2能与NaOH溶液反应)
(3)玻璃管A中发生反应的化学方程式为________________________,用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是________________.
(1)利用所学化学知识回答下列问题.
①碘酒是家庭常备药,碘酒中的溶剂是 (写名称).
②炎热的夏季,自行车轮胎容易爆胎,从微观角度分析,其原因是 .
③古代一些书法家、画家用墨书写或绘制的字画能保存很长时间而不变色的原因是 .
④小明书写的一个不正确的化学方程式:氧化汞加热分解
,请你检查后说出不正确的理由是 .
(2)下列句子中描述物质物理性质的是 (填序号),描述物质化学性质的是 (填序号).
①标准状况下,氧气是没有颜色,没有气味的气体.
②水受热沸腾时能变成水蒸气.
③二氧化碳能使澄清石灰水变浑浊.
④铁的密度是7.86g/cm3,熔点是1535℃.
(3)向盛有氢氧化钠溶液的烧杯中滴入酚酞溶液,溶液变为红色,此时溶液的pH 7(填">"、"<"或"="),向烧杯中逐滴加入稀盐酸,并不断搅拌至溶液颜色恰好变为 色,说明氢氧化钠与稀盐酸已反应,若继续滴入稀盐酸,烧杯中溶液的pH将 (填"升高"、"降低"或"不变")
如图是液态二氧化碳灭火器,据此回答下列问题.
(1)图中所标物质中钢属于 (填"金属材料"或"有机合成材料").
(2)加压在小钢瓶中的液态二氧化碳喷出后能灭火,其原理是 和 .
(3)在钢瓶表面涂油漆的作用是 .
(4)下列各组材料和试剂能够比较出铁和铜的金属活动性强弱的是 (填序号,合理选项有几项选几项).
| A. | 铁丝、钢丝、稀盐酸 | B. | 铁丝、硫酸铜溶液 | C. | 钢丝、硫酸亚铁溶液 | D. | 铁丝、钢丝、硫酸铝溶液. |

(1)化学用语是学习化学的关键,请用化学用语填空:
①镁原子 ;②硝酸根离子 ;③氮气 ;④氧化铝中铝元素的化合价为+3价 .
(2)符号"4
"中数字的含义:①"4"表示 ;②"2"表示 .
下图为某反应过程中,同一容器内反应前后物质种类的微观示意图。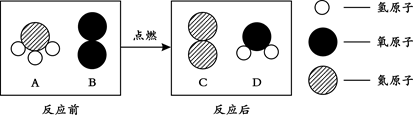
(1)上述四种物质中,属于氧化物的是(填字母)
(2)一个A分子中含有个原子。该物质中N、H两种元素的质量比为。
(3)该反应中,发生反应的A与B的微粒个数比为。
如图是铁丝在氧气中燃烧的实验,回答下列问题:
(1)现象:铁丝在氧气中剧烈燃烧,_____ ____ ,生成色固体;
(2)集气瓶内预留少量水目的是__________ _______;
(3)反应的化学方程式为___________,属于___________反应;
(4)若将氧气换成空气,则该反应__________进行(填“能”或“不能”)。