硝酸铵(NH4NO3)是一种常见的氮肥,请通过计算回答:
(1)硝酸铵的相对分子质量为________.
(2)硝酸铵中氮元素、氢元素、氧元素的质量比为________.
(3)某花卉基地需要配制100kg 10%的硝酸铵溶液,基地的实验室中现有200kg 5%的硝酸铵溶液和50kg 30%的硝酸铵溶液,若选用这两种溶液混合配制,应该如何进行?
现有一瓶久置的过氧化氢溶液(标签如图所示)。已知过氧化氢溶液在存放过程中会缓慢分解。取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。
请计算:
(1)现该瓶溶液的溶质质量分数。
(2)用该瓶溶液配制100g溶质质量分数为3%的过氧化氢溶液需要加入水的质量。
钛(Ti)是广泛应用于航空、航海等领域的一种重要金属。在一定条件下,钛由四氯化钛(TiCl4)和金属镁反应而制得:TiCl4+2Mg==Ti+2MgCl2 。现有380kg四氯化钛,计算可生产金属钛的质量。
钛(Ti)是一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。在一定条件下,钛可以由四氯化钛(TiCl4)和金属镁反应而制得:TiCl4 + 2Mg  Ti + 2MgCl2。现有380kg四氯化钛,可生产纯度为95%的金属钛多少千克?
Ti + 2MgCl2。现有380kg四氯化钛,可生产纯度为95%的金属钛多少千克?
星期天,小强的妈妈要焙制面包,叫取商店买回一纯碱,仔细看了装说明(如图),并产生疑问:
回到学校,他取出从家里带来的一小包纯碱样品进行实验:准确称取5.5g样品放入烧杯中,在滴加盐酸至刚好完全反应(忽略CO2溶于水),共用去稀盐酸25g,得溶液质量为28.3g(杂质溶于水且与盐酸不反应)。求: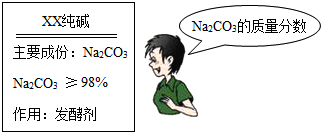
(1)生成CO2的质量是g。
(2)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符。(计算结果精确到0.1%)
小明在老师的指导下粗略测量一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数约为1%的氢氧化钠溶液。
步骤二:向10克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使
用pH计记录溶液的pH变化情况,绘制图像如图。
(1)在“步骤一”中有计算、、溶解三个具体步骤。
(2)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,在a点的溶液中
的微粒有。(用化学符号表示)
(3)请结合右图,计算①该稀盐酸的溶质质量分数;②b点时溶液中溶质的质量分数。(结果精确到0.1%)(写出计算过程)