下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.常温常压下,11.2L氯气含有的分之数为0.5NA |
| B.常温常压下,1mol氮气含有的质子数为7NA |
| C.在标准状态下,22.4LH2O含有的原子数目为3NA |
| D.32gO2所含原子数目为2NA |
现有乙酸和两种链状单烯烃混合物,其中氧的质量分数为a ,则碳的质量分数是:
A.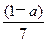 |
B.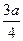 |
C.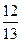 (1-a) (1-a) |
D.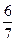 (1-a) (1-a) |
某有机物结构式为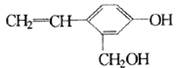 ,它不可能具有的性质是:
,它不可能具有的性质是:
①可以燃烧 ②能使酸性高锰酸钾溶液褪色 ③能跟KOH溶液反应 ④能发生聚合反应 ⑤能发生消去反应 ⑥能与金属钠反应 ⑦能发生取代反应 ⑧能被氧化
| A.①⑤⑦ | B.①②③④⑥⑦⑧ |
| C.⑤ | D.⑤⑧ |
能够鉴定溴乙烷中存在溴元素的实验操作是:
| A.在溴乙烷中直接加入AgNO3溶液 |
| B.加蒸馏水,充分搅拌后,加入AgNO3溶液 |
| C.加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液 |
| D.加入NaOH的乙醇溶液,加热后加入AgNO3溶液 |
某有机物的核磁共振氢谱图如下,该物质可能是: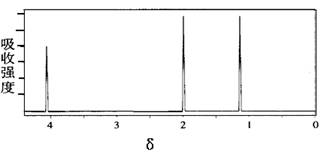
| A.乙酸 | B.苯酚 | C.丙醇 | D.乙酸乙酯 |
已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应为:
2CH3CH2Br + 2Na →CH3CH2CH2CH3 + 2NaBr
利用这一反应,下列所给化合物中可以与钠反应合成环丁烷的是:
| A.CH3Br | B.CH2BrCH2CH2CH2Br |
| C.CH2BrCH2Br | D.CH3CH2CH2CH2Br |