(重庆)工业上采用离子交换膜电解槽电解饱和食盐水,可以得到高浓度的烧碱溶液(含NaOH35%~48%).某学习小组为了验证附近氯碱化工厂产生的NaOH溶液是否达到高浓度标准,进行了如下操作,请你参与计算:
(1)到工厂采集了电解槽中的NaOH溶液100g.NaOH中氧元素的质量分数是________.
(2)在实验室用如图所示浓硫酸配制200g 24.5%的稀硫酸,计算所取浓硫酸的体积(计算结果取整数).
(3)进行中和测定,向采集到的溶液中逐渐加入所配制的稀硫酸,并不断测定溶液的pH,当pH=7时,消耗稀硫酸160g.通过计算判断此时电解槽中NaOH溶液是否达到高浓度标准.
(9分)碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业。有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如下图所示。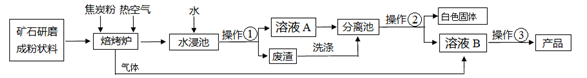
【已知】:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应。但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度。
| 温度/℃ |
0 |
40 |
80 |
| Ca(OH)2溶解度/g |
0.187 |
0.141 |
0.094 |
| Ba(OH)2溶解度/g |
1.67 |
8.22 |
101.4 |
(1)矿石研磨成粉末的目的_______________
(2)以下相关说法正确的是。
A.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
B.焙烧炉内只涉及分解反应
C.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料
(3)写出焙烧炉中含钡元素物质发生反应的化学方程式;
(4)除了水之外,进入分离池中的物质是和,请你推测分离池中操作②的方法是(选填“A”或“B”)。
A.降温,过滤;B.加热,过滤
(5)写出由溶液B制取产品的化学方程式:;
(6)若此矿石原料50t,得到的产品质量为19.7t , 则此矿石中钡元素的质量分数__________(写出计算过程,共2分)
某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验室技术员称取6.25 g研碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体质量的重复操作,记录数据如下:(提示:碳酸钙在高温下分解,生成氧化钙和二氧化碳气体)
| 操作次序 |
第一次 |
第二次 |
第三次 |
第四次 |
| 剩余固体质量 |
5.55g |
4.35g |
4.05g |
4.05g |
试计算:
(1)完全反应后生成二氧化碳 g;
(2)石灰石样品中碳酸钙的质量分数(计算结果精确到0.1%)。
(6分)为了节约林木资源,近几年兴起了石头纸.石头纸可用沿海水产养殖中产生的大量废弃贝壳制得,为了测定某种贝壳中碳酸钙的质量分数,取贝壳25g,加入200g的稀盐酸,恰好完全反应,称得反应后物质的总质量为216.2g(假设贝壳中其它物质不与盐酸反应且不溶于水).请你计算:
(1)贝壳中碳酸钙的质量分数;
(2)反应后所得溶液中溶质的质量分数(精确到0.1%).
(2分)环氧化(R)丙烯醇(化学式为C3H6O2)是沙普利斯教授应用不对称合成技术合成的一种重要物质。该物质用于生产一种治疗心脏病的药物。计算:
(1)C3H6O2中的碳、氢、氧三种元素的质量比;
(2)C3H6O2中碳元素的质量分数。(精确到0.1%)
某化工厂排放的废水中只含有盐酸和MgCl2两种物质。小明同学向采集来的62.8 g废水样品中,慢慢加入20%的NaOH溶液至恰好完全反应时,消耗NaOH溶液60g。将生成的沉淀物过滤出,经水洗、干燥后称重为5.8g。
求:废水中盐酸的质量分数