硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:
已知:(ⅰ)PbCl2(s)+2Cl-(aq) PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
(ⅱ)有关物质的Ksp和沉淀时的pH如下:
| Ksp |
|
开始沉淀时pH |
完全沉淀时pH |
|
| PbSO4 |
1.08×10-8 |
Fe (OH)3 |
2.7 |
3.7 |
| PbCl2 |
1.6×10-5 |
Pb(OH)2 |
6 |
7.04 |
(1)步骤Ⅰ中生成PbCl2的离子方程式_______,加入盐酸控制pH值小于2,原因是_______。
(2)用化学平衡移动原理解释步骤Ⅱ中使用冰水浴的原因______。若原料中FeCl3过量,则步骤Ⅱ得到的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是_______。
(3)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式______。
(4)请用离子方程式解释滤液2加入H2O2可循环利用的原因______。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为_______。
(6)双隔膜电解池的结构示意简图如图所示,利用铅蓄电池电解硫酸钠溶液可以制取硫酸和氢氧化钠,并得到氢气和氧气。对该装置及其原理判断正确的是____。
A.A溶液为氢氧化钠,B溶液为硫酸
B.C1极与铅蓄电池的PbO2电极相接、C2极与铅蓄电池的Pb电极相接
C.当C1极产生标准状况下11.2 L气体时,铅蓄电池的负极增重49g
D.该电解反应的总方程式可以表示为:2Na2SO4+6H2O 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑
有A、B、C、D四种短周期主族元素,其原子序数依次增大。A、B可形成A2B和A2B2两种共价化合物,B、C同主族且可形成CB2和CB3两种化合物。完成下列问题。
(1)C的名称为________
(2)写出表示非金属性C<D的化学方程式(任一个):________。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中,溶液由黄色逐渐变为浅绿色,该反应的离子方程式为___________。
(4)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出负极反应式。
负极反应式:____________________。
I(1)某同学做如下实验,以检验反应中的能量变化。
实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是__________热反应;(b)中温度降低, 根据能量守恒定律,(b)中反应物的总能量应该__________其生成物的总能量。
(2)下列反应:①氢氧化钠与硫酸,②一氧化碳与氧气,③八水合氢氧化钡与氯化铵,④金属铜与硝酸银。其中(用序号填空):
能设计成原电池的反应是____________________________________________。
II(1)有下列几种物质
A.金刚石和石墨
B.C2H6和C5H12
C.C2H4和C2H6
D.CH3CH2CH2CH3和CH3CH(CH3)2
E.35Cl和37Cl
属于同分异构体的是________;属于同素异形体的是________;属于同系物的是________;属于同位素的是________。
(2)两种粒子的核外电子排布相同,核电荷数不同,则它们可能是( )
A.两种不同元素的原子 B.一定是两种不同的离子
C.同一元素的原子和离子 D.两种不同元素的原子和离子
III:(1)C7H16名称
(2)指出下列反应的类型
乙烯使酸性高锰酸钾溶液褪色:_________________
(3)写出反应的化学方程式:三氯甲烷与氯气在光照下反应_________________
已知NO2和N2O4之间发生可逆反应: 2NO2 (g) (红棕色) N2O4(g) (无色)
N2O4(g) (无色)
(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。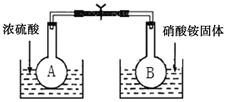
分别向两个烧杯中加入浓硫酸和NH4NO3固体,观察到的现象是:A中气体红棕色加深,B中 。这说明,当条件改变时,原来的化学平衡将被破坏,并在新的条件下建立起新的平衡,即发生。
(2)下图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2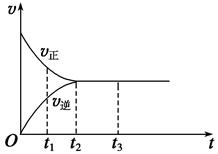 气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是。
气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是。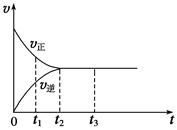
a.t1时,反应未达到平衡, NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等
e.0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
(3)某容积2L的密闭容器中充入一定量的NO2和N2O4的混合气体,在一定温度压强下,两者物质的量随时间变化如图所示。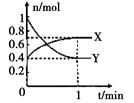
①表示NO2变化的曲线是(填“X”或“Y”)。
②在0到1 min内用Y的浓度变化表示的该反应的
反应速率是mol·L-1·min-1
下图为元素周期表的一部分,请根据元素①~⑧在表中的位置,回答下列问题:

(1)在上述元素的最高价氧化物对应的水化物中:属于强酸的是(用化学式表示,下同);碱性最强的是。
(2)④、⑤、⑥的简单离子半径由大到小的顺序是(用离子符号表示)。
(3)有两种离子化合物,均由①、④、⑤、⑧四种元素组成,这两种物质可在水溶液中发生反应。写出该反应的离子方程式:。
(4)请写出涉及上述有关元素的两个置换反应(要求:同一反应中两种单质对应元素既不同周期也不同主族);
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
若A、B、C含同一金属元素,X为强电解质,且反应都在溶液中进行。B的化学式为。
X的化学式可能为(写出不同类物质)或。
原子序数由小到大排列的四种短周期元素X、Y、 Z、W, 四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)M元素是__________(填元素符号)。
(2)Z、W形成的气态氢物的稳定性为_______>________。(填化学式)
(3)写出M完全燃烧生成的氧化物的电子式________,该氧化物与水反应的离子方程式________。
(4)由X、Y、Z、W四种元素中的三种组成的—种强酸,该强酸的稀溶液能与铜反应,离子方程式为_______。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1molA能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是_______(填化学式)。写出该气体B与氯水反应的离子方程式____________________。
(6)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物C,1mol C中含有6mol结晶水。对化合物C进行下实验:a.取C的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;b.另取C的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。C的化学式为______________________________。