已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应
Ⅰ:WO42-(aq) + Ca(OH)2(s)  CaWO4(s) + 2OH-(aq)。
CaWO4(s) + 2OH-(aq)。
(1)下图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。
①计算T1时KSP(CaWO4)= ________。
②T1________ T2(填“>”“=”或“<”)。
(2)反应Ⅰ的平衡常数K理论值如下表:
| 温度/℃ |
25 |
50 |
90 |
100 |
| K |
79.96 |
208.06 |
222.88 |
258.05 |
①该反应平衡常数K的表达式为________。
②该反应的△H________0(填“>”“=”或“<”)。
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4) =" c(NaOH)" =" 0.5" mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后WO42—的沉淀率为60%,计算实验测得的平衡常数。
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,分析其作用:________。
月桂烯( 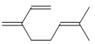 )是重要的化工原料,广泛用于香料行业。
)是重要的化工原料,广泛用于香料行业。
(1)月桂烯与足量氢气完全加成后生成A,A的名称是;
(2)以月桂烯为原料制取乙酸香叶酯的流程如下图: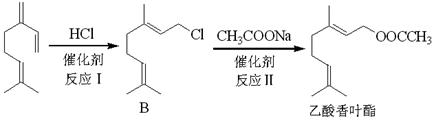
①B中官能团的名称;
②乙酸香叶酯的化学式;
③反应Ⅰ的反应类型是;
④反应Ⅱ的化学方程式是;
(3)已知:烯烃臭氧化还原水解反应生成羰基化合物,如: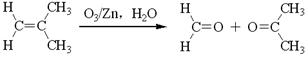
一定条件下,月桂烯可实现如下图所示转化(图中部分产物已略去):
①C与新制的Cu(OH)2悬浊液反应的化学方程式为:
;
②E在一定条件下能发生缩聚反应,写出其产物的结构简式。
已知有机物之间能发下如下反应: 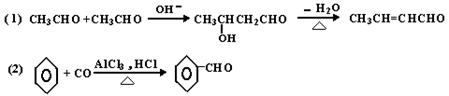
下列有机化合物A~H有如下图所示的转化关系: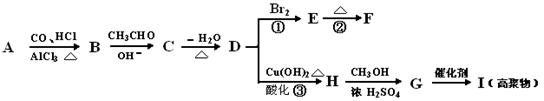
其中,化合物D的分子式为C10H10O,其苯环上的一氯代物只有两种;F的分子式为C10H8O,且所有碳原子在同一平面上。请回答下列问题:
(1)写出下列物质的结构简式:A ;I。
(2)反应①的反应类型为;反应②的条件为。化合物F的核磁共振氢谱(1H-NMR)显示有个峰。
(3)写出下列反应的化学方程式:
CH3CHO与足量HCHO反应。
反应③。
(4)化合物D有多种同分异构体,满足下列条件的有6种(一个碳原子上不可能两个双键):①属于酚类;②结构中除苯环外无其他环;③苯环上只有两种互为对位的取代基。
其中的三种结构简式如下:
请写出其它三种结构简式、、。
高分子化合物PBT和顺丁橡胶CBR的合成路线如下(部分产物及反应条件略):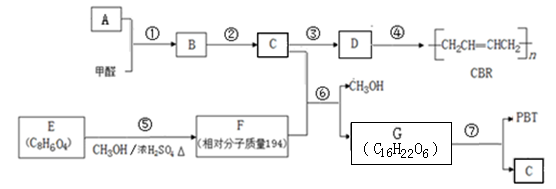
已知:ⅰ.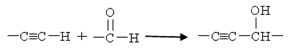
ⅱ.RCOOR'+ R"18OH  RCO18OR"+ R'OH
RCO18OR"+ R'OH
(1)已知④属于加聚反应,则D的分子式是。
(2)实验室常用电石和水反应制备A,A的名称是。
(3)B中所含官能团的名称是。
(4)③的反应类型是。
(5)E为芳香族化合物,其苯环上的一氯代物只有一种。⑤的化学方程式是。
(6)E有多种芳香族同分异构体,其中红外光谱显示分子中含“-COO-”,核磁共振氢谱显示3个吸收峰,且峰面积之比为1︰1︰1的同分异构体有种,写出其中任一种的结构简式:。
(7)⑦的化学方程式是。
根据Fe3++ Ag  Fe2+ + Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
Fe2+ + Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
(1)FeCl3溶液显酸性,原因是(用离子方程式表示)。
(2)关于FeCl3溶液洗银后的相关叙述正确的是(填序号)。
a.c(Fe3+)减小 b.c(Cl-)不变 c.铁元素质量减小
(3)Fe(NO3)3溶液洗银时,甲同学认为NO3-也能将银氧化。他认为可以通过检验Fe(NO3)3溶液洗银后NO3-的还原产物来判断NO3-是否能将银氧化,而乙同学认为此方法不可行,乙同学的理由是。
(4)乙同学欲从洗银废液(Fe3+、 Fe2+、 Ag+、 NO3-)中回收银和刻蚀液,设计了如下路线: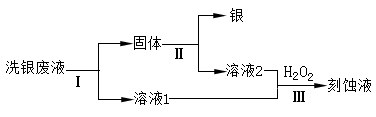
①过程Ⅰ中反应的离子方程式是。
②过程Ⅱ中加入的试剂可以是。
(5)镀银后的银氨溶液放置时会析出有强爆炸性的物质,所以不能贮存。从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①生成AgCl沉淀的化学方程式是。
②若该反应中消耗3.3 g羟氨,理论上可得银的质量为g。
元素铝是在生产、生活中应用广泛的金属元素。
(1)从矿石提取氧化铝:矿石与NaOH溶液高温反应,然后降温析出晶体,再经净化和高温煅烧得到氧化铝。降温析出晶体时的反应方程式为:。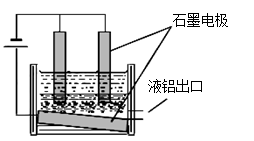
(2)氧化铝是工业电解冶炼铝的重要原料,生产中加入冰晶石(Na3AlF6),其作用是。
工业冶炼铝的装置示意图如右:
①阴极的反应式,
②在电解池工作过程中,需要不断补充阳极材料,原因是。
(3)有资料介绍:溶液中铝元素以氢氧化物[用Al(OH)3表示]形式存在的pH范围是3.8~10。现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为。
(4)一种新型高效净水剂PAFC——聚合氯化铁铝[A1Fe(OH)nCl6-n]m,广泛用于日常生活用水和工业污水的处理。有关PAFC的说法正确的是。(填选项)
A.PAFC中铁元素显+2价
B.PAFC用于净水时,比用相同量的氯化铝和氯化铁对水的pH改变小
C.PAFC可看作一定比例的氯化铁与氯化铝水解的中间产物
D.PAFC在强酸性和强碱性溶液中都能稳定存在