(1)由金红石(TiO2)制取单质Ti涉及的步骤为:TiO2→TiCl4 Ti。
Ti。
已知:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) TiCl4(s)+O2(g) ΔH3=+141 kJ·mol-1
TiCl4(s)+O2(g) ΔH3=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s) TiCl4(s)+2CO(g)的 ΔH= 。
TiCl4(s)+2CO(g)的 ΔH= 。
(2)在一定温度下,5L密闭容器中进行TiO2(s)+2Cl2(g)+2C(s) TiCl4(s)+2CO(g)反应,若容器中加入足量的TiO2和C后,充入0.2mol的Cl2,经过5s达到平衡时Cl2转化率为80%。
TiCl4(s)+2CO(g)反应,若容器中加入足量的TiO2和C后,充入0.2mol的Cl2,经过5s达到平衡时Cl2转化率为80%。
①计算v(CO)= mol/(L·s) ,此温度下的平衡常数K= 。
②用Cl2的物质的量浓度的改变来表示反应速率v正、v逆与时间的关系图,则图中阴影部分的面积为 。
③以下各项不能说明该反应达到平衡状态的是 。
| A.气体的密度不随时间改变 |
| B.容器中的压强不随时间变化 |
| C.CO的浓度不随时间变化 |
| D.TiCl4物质的量不随时间变化 |
E. TiCl4与CO物质的量之比不随时间变化
④若继续充入0.2molCl2,重新达到平衡后Cl2的浓度为 mol/L。
(3)反应③经过10 min达到平衡,得到物质的量浓度与时间的关系如下图。若将容器的容积压缩为原来的一半,再经过5 min后重新达到平衡时的平衡常数为 ,若升高温度该反应的平衡常数将 (填:增大、减小或不变)。
下表为元素周期表短周期的一部分。回答下列问题:
| A |
D |
|||
| E |
G |
M |
(1)E元素原子核外有2个未成对电子,这2个电子所处亚层的符号是;请从物质的类别、化合价二方面归纳该元素+4价氧化物的化学性质:。
(2)请指出G的非金属性比E的非金属性强的事实(写3)。 (3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释。
(3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释。
(4)A与氢元素形成分子的空间结构可能是(选填序号)。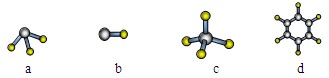
有浓度为0.1 mol•L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol·L-1,b mol·L-1,c mol·L-1,其大小顺序为__________。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为
n 1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为____________。
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其大小关系为____________。
若以铁棒、碳棒、导线和氯化铁溶液为用品设计原电池。电池反应式为_________________________。
某温度(t℃)时,水的KW=10-13则该温度(填大于、等于或小于)______25℃,理由是________________________________________________
依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。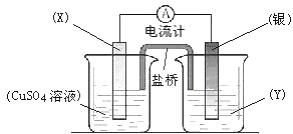
请回答下列问题:
(1)电极X的材料是_________;电解质溶液Y是_________;
(2)银电极为电池的_________极,发生的电极反应为________________________;X电极上发生的电极反应为___________________________;
(3)外电路中的电子是从_________电极流向_________电极。