【化学——选修3 物质结构与性质】A,B,C,D,E五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57;B原子的L层P轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同,E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)B,D可分别与A形成只含一个中心原子的共价化合物X和Y,其中X的电子式为 ;Y采取的杂化轨道类型为 ;C与A形成的常见化合物的分子构型为 。
(2)B和D的最高价氧化物的晶体中熔点较高的是(填化学式) ,其原因 。
(3)B与C比较电负性较大的是 (填元素符号),E2+的核外电子排布式为 。
(4)E2+与C的常见氢化物形成的配离子的离子反应方程式为 。
(5)铝单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。若已知铝原子半径为d,NA表示阿伏加德罗常数,摩尔质量为M,则该原子的配位数 ,该晶体的密度可表示为______________,据下图计算,Al原子采取的面心立方堆积的空间利用率为 __________。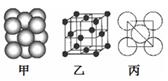
用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100 mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50
mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50 mL烧杯;应选用的仪器有(填编号)。
mL烧杯;应选用的仪器有(填编号)。
(2)应称取Na2CO3的质量为。
实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①取25mL甲溶液, 向其中缓慢滴入乙溶液15mL,共收集到112mL(标准状况)气体。
向其中缓慢滴入乙溶液15mL,共收集到112mL(标准状况)气体。
②取15mL乙溶液,向其中缓慢滴入甲溶液25mL,共收集到56mL(标准状况)气体。
(1)判断:甲是溶液,乙是溶液;(均填化 学式)
学式)
(2)②实验中所发生反应的离子方程式为:
;
(3)甲溶液的物质的量浓度为mol/L,乙溶液的物质的量浓度为mol/L
现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。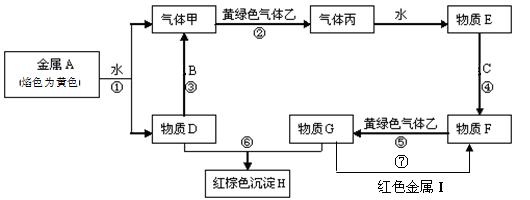
请根据以上信息回答下列问题:
(1)写出下列物质的化学式: C、H
(2)写出反应①的离子方程式:。
写出反应⑦的离子方程式:。
(3)实验室检验物质G中阳离子的常用试剂是:。
SO3和SiO2均属于酸性氧化物,能溶于水的是_________,反应的化学方程式是___________________________;SiO2与氢氟酸(HF的水溶液)反应,常用于刻蚀玻璃,该反应的化学方程式是_________________________________。请写出Al2O3分别与盐酸、氢氧化钠溶液反应的离子方程式:____________________________,___________________________________,所以Al2O3属于______氧化物。
(1)白色的Fe(OH)2在空气中发生的颜色变化为________________________;
(2)写出硅酸钠溶液在空气中变质的化学方程式:____________________________;
(3)写出用熟石灰吸收氯气制漂白粉的化学方程式:;
(4)将CaMg3Si4O12改写为氧化物的形式:__________________________________。