下列离子方程式表达正确的是
| A.碘化亚铁溶液中通入少量氯气:Cl2+2Fe2+=2Fe3++2Cl— |
| B.向1mol/L 0.1L的明矾溶液中加入0.5mol/L 0.2L的Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C.将蛋壳浸泡到醋酸中:CO32—+2CH3COOH=2CH3COO—+ CO2↑+H2O |
| D.将过氧化钠与水反应:2O22—+2H2O=O2+4OH— |
已知298K下反应2Al2O3(s)+3C(s)==4Al(s)+3CO2(g) ΔH=+2171kJ·mol-1
△S=+635.5J·mol-1·K-1,则此反应
| A.高温下可自发进行 | B.任何条件下都可自发进行 |
| C.任何条件下都不可自发进行 | D.低温下可自发进行 |
相同物质的量的下列物质分别与等浓度的足量的NaOH溶液反应,消耗碱量最多的是
| A.Al2O3 | B.Al(OH)3 | C.AlCl3 | D.Fe(NO3)3 |
某温度下,可逆反应m A(g) +n B(g) 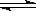 p C(g)的平衡常数为K,下列对K的说法正确的是
p C(g)的平衡常数为K,下列对K的说法正确的是
| A.K值越大,表明该反应越有利于C的生成,反应物的转化率越大 |
| B.若缩小反应器的容积,能使平衡正向移动,则K增大 |
| C.温度越高,K一定越大 |
| D.如果m+n==p,则K=1 |
电解稀H2SO4、Cu(NO3)2、NaCl的混合液,最初一段时间阴极和阳极上分别析出的物质分别是
| A.H2和Cl2 | B.Cu和Cl2 | C.H2和O2 | D.Cu和O2 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是
A.反应的化学方程式为:N 2M 2M |
| B.t1分钟内,反应速率: v(M)=2v(N) |
| C.t 2时,正逆反应速率相等,达到平衡 |
| D.平衡时,N的转化率是75% |