还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下: ,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
,已知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)==Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
| A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g |
| B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态 |
| C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5 |
下列与有关非金属元素叙述以及推理结果不正确的是()
①非金属性F>Cl,故将F2通入NaCl溶液中,发生反应为:F2 + 2Cl-= Cl 2 + 2F-
②非金属性F>Br,故酸性:HF>HBr
③非金属性S>As ,故前者的气态氢化物稳定性更强
④非金属性O>N,故O 2与H2化合比N2更容易
| A.②③ | B.③④ | C.①④ | D.①② |
已知反应X+Y= M+N为吸热反应,对这个反应的下列说法中正确的是()
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
下列各组化合物中,化学键类型完全相同的是()
| A.CaCl2和 Na2S | B.Na2O 和Na2O2 | C.CO2和 CaO | D.HCl 和NaOH |
以苯为原料,不能通过一步反应而制得的有机物是( )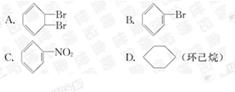
某气态的烷烃与烯烃的混合气体9 g,其密度为同状况下H2密度的11.2倍,将混合气体通过足量的溴水,溴水增重4.2 g,则原混合气体的组成为( )
| A.甲烷,乙烯 | B.甲烷,丙烯 | C.乙烷,乙烯 | D.甲烷,丁烯 |