下列解释实验事实的方程式正确的是
A.纯碱溶液可以清洗油污的原因 CO32¯+2H2O H2CO3+2OH¯ H2CO3+2OH¯ |
| B.在强碱溶液中NaClO与Fe(OH)3反应制备Na2FeO43ClO¯ + 2Fe(OH)3 + 4OH¯ = 2FeO42¯ + 3Cl¯+ 5H2O |
| C.铜制品表面的水膜酸性较强时,发生电化学腐蚀,正极反应为2H++2e-=H2↑ |
| D.向AgNO3溶液中加过量NaCl后再加Na2S溶液,白色沉淀变黑色 2Ag++S2¯= Ag2S↓ |
酸性条件下20mL 0.5mol/L的KMnO4溶液可将25 mL 2 mol/L的FeSO4溶液中的Fe2+恰好完全氧化为Fe3+,则KMnO4被还原的产物是
| A.K2MnO4 | B.Mn2O3 | C.MnO2 | D.Mn2+ |
下列化学反应的离子方程式正确的是
A.用小苏打治疗胃酸过多:HCO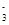 +H+=CO2↑+H2O +H+=CO2↑+H2O |
B.往碳酸镁中滴加稀盐酸:CO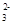 +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| C.往澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
D.氢氧化钡溶液与稀硫酸反应: Ba2++SO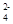 +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
下列各组离子中,能在强酸性溶液里大量共存,并且溶液呈无色透明的是
A.Fe3+、K+、Na+、SO |
B.Mg2+、Na+、Cl-、NO |
C.Na+、K+、CO 、Cl- 、Cl- |
D.Ba2+、K+、HCO 、SO 、SO |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.标准状况下,11.2LH2O中含有的分子数目为0.5NA |
| B.25℃,1.01×105Pa,64gSO2中含有的原子数为3NA |
| C.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
| D.标准状况下,22.4L N2和H2混合气中含NA个原子 |
下列四幅图中,小白球代表的是氢原子,大灰球代表的是氦原子。最适合表示同温同压下,等质量的氢气与氦气的混合气体的图示是
A B C D