实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种.为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论):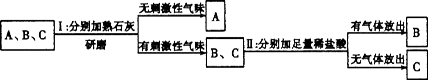
根据上述实验回答:
(1)写出三种化肥的名称:A________;B________;C________.
(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果________(填“有”或“无”)影响.
(3)常温下如要鉴别B、C两种样品,________(填“能”或“不能”)采取闻气味的方法.
(4)由实验和查阅资料可知,人们在施用铵态氮肥时,若遇到碱性物质,会使铵态氮肥转化为氨气,氨气进入大气后与雨水作用,可能形成“碱雨”.“碱雨”中碱的化学式为________.
化学为交通运输做出很多贡献。请回答下列问题:
(1)汽车在行驶过程中的能量转化是__________________________;
(2)飞机外壳用的主要材料是硬铝,它属于_______(填序号);
A.合成材料B.金属材料C.复合材料
(3)载人航天飞船所用固体燃料是铝粉和高氯酸铵(NH4ClO4)的混合物。发射时,点燃铝粉产生大量的热,达到高温,引起高氯酸铵发生分解,产生空气中含量最多的两种气体、一种常见的液态氧化物和氯气。写出高氯酸铵分解的化学方程式___________________,该反应前后氮元素的化合价变化为_________。
金属及其制品是现代生活中常见的材料,请回答下列问题:
(1)铁和铝都可以制作炊具,主要利用了它们的 性.
(2)金属锌可以提取AgNO3废水中的银,这是因为锌的活动性比银 .
(3)将生铁加入足量的稀盐酸中,充分反应后得到浅绿色溶液,该溶液中含有的金属离子主要是
(写符号),溶液底部残留的黑色不溶物主要是 .
将4.0gCu–Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应。过滤、称量滤液的质量。相关实验数据如下:
| 反应前物质的质量 / g |
反应后物质的质量 / g |
|
| Cu – Zn合金 |
稀硫酸 |
滤液 |
| 4.0 |
10 |
11.26 |
(1)Cu – Zn合金属于 材料(“金属”或“有机合成”)
(2)若不考虑该合金中除Cu、Zn以外的其他成分,请计算原Cu – Zn合金中Zn的质量。写出必要的计算过程。
为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
| 反应前 |
反应后 |
||
| 实验数据 |
烧杯和稀盐酸的质量 |
纯碱样品的质量/g |
烧杯和其中混合物的质量/g |
| 120 |
12 |
127.6 |
|
请计算:(1)该反应生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数为多少。(请写出计算过程)
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂说明书的部分信息如图所示。
现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关信息回答问题。
| 第1次 |
第3次 |
第4次 |
|
| 加入盐酸的质量(g) |
20 |
20 |
20 |
| 剩余固体的质量(g) |
35 |
a |
20 |

(1) 人体缺钙易出现的疾病是 ,这时除在医生指导下服用保健药剂外,日常生活中要多摄入 等食物。
人体缺钙易出现的疾病是 ,这时除在医生指导下服用保健药剂外,日常生活中要多摄入 等食物。
(2)该品牌补钙药剂中CaCO3的质量分数是 ,a的数值为 。
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)。