一定量的与足量的碳在体积可变的恒压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如下图所示:
。平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(P分)=气体总压(P总)×体积分数。下列说法正确的是
| A. | 550 时,若充入惰性气体, 正, 逆 均减小,平衡不移动 |
| B. | 650 时,反应达平衡后 的转化率为25.0% |
| C. | 时,若充入等体积的 和 ,平衡向逆反应方向移动 |
| D. | 925 时,用平衡分压代替平衡浓度表示的化学平衡常数 =24.0P 总 |
将 4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)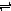 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol•L-1,
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol•L-1,
现有下列正确的是
| A.用物质 B 表示的反应的平均速率为 0.6 mol•L-1•s-1 |
| B.2 s 时物质 B 的浓度为 0.7 mol•L-1 |
| C.2 s 时物质 A 的转化率为70% |
| D.用物质 A 表示的反应的平均速率为 0.3 mol•L-1•s-1 |
下列有关防护金属腐蚀的说法中,不正确的是
| A.青铜(锡铜合金)中的锡可对铜起保护作用 |
| B.在海轮外壳上焊接上锌块,可减缓船体的腐蚀速率 |
| C.钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀的作用 |
| D.海水中钢闸门与电源的正极相连,可以防止闸门的腐蚀 |
右图为一原电池的结构示意图,下列说法中,错误的是 
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
下列方法能使电离平衡H2O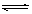 H+ + OH-向右移动,且使溶液呈酸性的是
H+ + OH-向右移动,且使溶液呈酸性的是
| A.向水中加入少量硫酸铝固体 | B.向水中加入少量硫酸氢钠固体 |
| C.向水中加入少量碳酸钠固体 | D.将水加热到100℃,使水的pH=6 |
有一处于平衡状态的反应:X(s)+3Y(g)  2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加正催化剂 ⑥分离出Z
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |