海水开发利用的部分过程如图所示。下列说法错误的是

| A. | 向苦卤中通入 是为了提取溴 |
| B. | 粗盐可采用除杂和重结晶等过程提纯 |
| C. | 工业生产中常选用 作为沉淀剂 |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收 |
反应 4NH3(g)+5O2(g)  4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为
| A.v(NH3) ="0.010" mol/(L·s) | B.v(O2)="0.001" mol/(L·s) |
| C.v(NO) ="0.0010" mol/(L·s) | D.v(H2O) ="0.045" mol/(L·s) |
具有解热镇痛及抗生素作用的药物“芬必得”主要成分的结构简式为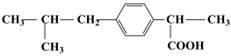 ,它属于
,它属于
①芳香族化合物 ②脂肪族化合物 ③有机羧酸 ④有机高分子化合物 ⑤芳香烃
| A.③⑤ | B.②③ | C.①③ | D.①④ |
下列物质中,属于“城市空气质量日报”报道的污染物是
| A.N2 | B.O2 | C.CO2 | D.SO2 |
已知Fe3O4可表示成FeO·Fe2O3,水热法制备Fe3O4纳米颗粒的总反应为: 3Fe2++2S2O32-+O2 +4OH-==Fe3O4+S4O62-+2H2O。下列说法正确的是( )
| A.O2和S2O32-是氧化剂,Fe2+是还原剂 |
| B.若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol |
| C.每生成1 mol Fe3O4,转移电子的物质的量为2 mol |
| D.参加反应的氧化剂与还原剂的物质的量之比为1∶1 |
向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
| A.原NaOH溶液的浓度为0.1mol/L |
| B.通入CO2的体积为448mL |
| C.所得溶液的溶质成分的物质的量之比为(NaOH):(Na2CO3)=1:3 |
| D.所得溶液的溶质成分的物质的量之比为(NaHCO3):(Na2CO3)=2:1 |