下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是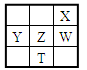
| A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 |
| B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 |
| C.YX2晶体熔化、液态WX3气化均需克服分子间作用力 |
| D.根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是()
①澄清石灰水中通过量的CO2;②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向AgNO3溶液中逐滴加入过量氨水; ④向硅酸钠溶液中逐滴加入过量的盐酸
| A.②④ | B.①③ | C.③④ | D.④ |
根据右图,可判断出下列离子方程式中错误的是()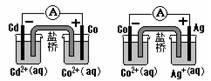
| A.2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s) |
| B.Cd (s)+Co2+(aq)=Cd2+(aq)+Co(s) |
| C.2Ag+ (aq)+Cd(s)=2Ag(s)+Cd(aq) |
| D.2Ag+ (aq)+Co(s)=2Ag(s)+Co(aq) |
NA为阿伏加德罗常数,下列叙述正确的是()
| A.反应5I—+IO3—+6H+ = 3I2 +3H2O生成3mol碘单质转移电子数为5NA |
| B.1 mol Na2O2溶于水作用时转移的电子数为2NA |
| C.在标准状况下,含NA个氦原子的氦气所含的分子数是0.5 NA |
| D.在7.8 g Na2O2晶体中阳离子与阴离子总数为0.4 NA |
下列实验方法、或除去杂质的方法正确的是()
| A.钠也可以保存在CCl4中 |
| B.钠着火时可以砂土来扑灭; |
| C.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
下列五种有色溶液通入SO2时均能褪色或变色,其实质相同的是()
①品红溶液 ②酸性KMnO4溶液 ③滴有酚酞的NaOH溶液
④溴水 ⑤石蕊溶液;⑥FeCl3溶液
| A.①④ | B.①③ | C.①②⑤ | D.②④⑥ |