与的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器的名称是。安装中导管时,应选用图2中的。
(2)打开的活塞,A中发生反应:+=↑+↑++。
为使在中被稳定剂充分吸收,滴加稀盐酸的速度宜 (填"快"或"慢")。
(3)关闭的活塞,在中被稳定剂完全吸收生成,此时中溶液的颜色不变,则装置的作用是。
(4)已知在酸性条件下NaClO2可发生反应生成并释放出,该反应的离子方程式为,在释放实验中,打开的活塞,中发生反应,则装置的作用是 。
(5)已吸收气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是,原因是 。

氨的合成原理为:N2(g)+3H2(g) 2NH3(g);△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
2NH3(g);△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题: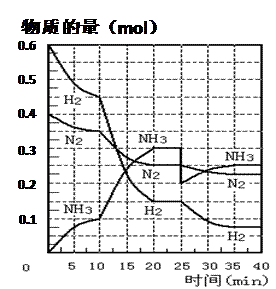
(1)10 min内以NH3表示的平均反应速率;
(2)在10 ~20 min内:NH3浓度变化的原因可能是;
| A.加了催化剂 | B.缩小容器体积 |
| C.降低温度 | D.增加NH3物质的量 |
(3)第1次平衡的时间范围为:,
第2次平衡的时间范围为:,
第1次平衡:平衡常数K1 = (带数据的表达式),
第2次平衡时NH3的体积分数;
(4)在反应进行至25 min时:
① 曲线发生变化的原因:
② 达第二次平衡时,新平衡的平衡常数
K2K1(填“大于”、“等于”、“小于”);
(5)在25~40 min时,计算合成氨过程中的反应热△H= 。
(6)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:
N2(g) + 3H2O(1) 2NH3(g) +
2NH3(g) +  O2(g);△H =" a" kJ·mol—1
O2(g);△H =" a" kJ·mol—1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K |
303 |
313 |
323 |
| NH3生成量/(10-6mol) |
4.8 |
5.9 |
6.0 |
①此合成反应的a0;ΔS0,(填“>”、“<”或“=”)
②已知:N2(g) + 3H2(g) 2NH3(g) ΔH= -92 .4kJ·mol—1
2NH3(g) ΔH= -92 .4kJ·mol—1
2H2(g) + O2(g) = 2H2O(l) = -571.6kJ·mol—1
则常温下氮气与水反应生成氨气与氧气的热化学方程式为:
实验室制配0.5 mol/L的NaOH溶液500 mL,有以下仪器:①烧杯 ②100 mL量筒 ③1000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥试管 ⑦药匙
⑴ 配制时,必须使用的仪器有___(填代号),
还缺少的仪器是_____。
⑵ 实验两次用到玻璃棒,其作用分别是: 、 。
⑶ 配制时,一般可分为以下几个步骤:①称量②计算 ③溶解 ④摇匀⑤转移 ⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为。
⑷ 试分析下列操作对所配溶液的浓度有何影响。(填“偏高”、“偏低”或“无影响” )
①定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,对所配溶液浓度的影响__________。
②某同学观察液面的情况如下图所示,则所配置的溶液的浓度______________。
⑸ 取出其中50ml溶液加水稀释到100ml,稀释后溶液中NaCl的物质的量浓度为____________________。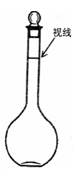
实验室要配制100mL、10mol·L-1的NaCl溶液,试回答下列各题:
(1)经计算,应该用托盘天平称取NaCl固体g。
(2)配制溶液时一般可分为以下几个步骤: ①称量②计算③定容
④移液 ⑤洗涤⑥溶解其正确的操作顺序为。
(3)(2分,每空1分)该实验两次用到玻璃棒,其作用分别是:
① 溶解时玻璃棒的作用② 移液时玻璃棒的作用
(4)容量瓶上需标有以下5项中的 ①温度 ②浓度 ③容量 ④压强 ⑤刻度线()
A.①③⑤ B.③⑤⑥ C.①②④ D.②④⑥
(5)(2分)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_____。(填序号)
A.蒸发皿 B.100mL容量瓶 C.烧杯 D.胶头滴管 E.药匙 F.托盘天平 G.玻璃棒
(6)(2分)下列错误操作会导致所得溶液浓度偏低的是(多项,填序号)。
A. 定容时仰视容量瓶刻度线
B.容量瓶中原有少量蒸馏水
C. 定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
D. 配制好溶液后,容量瓶未塞好,洒出一些溶液
利用铝热反应焊接钢轨的原理是2Al+Fe2O3 2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
2Fe+ Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褪褐色硬块的组成。
样品处理:将褐色硬块处理成粉末状。
(1)研究小组首先取少量粉末加入溶液中,发现粉末部分溶解,但没有气泡产生,实验结论是:粉末中含有Al2O3而没有Al。
(2)根据以述实验判断该褐色硬块的组成基本确定为Fe、Fe2O3、Al2O3。
提出假设:
假设1:固体粉末中除Al2O3外还有Fe;
假设2:固体粉末中除Al2O3外还有;
假设3:固体粉末中除Al2O3外还有Fe和Fe2O3。
实验实施:
(3)请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/LHCl、3mol/LHNO3、3mol/LCuSO4、0.01mol/LKMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。
| 实验操作 |
预期现象和结论 |
 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。 |
|
| 步骤2:将步骤1的滤渣转移到烧杯B中,加入足量,充分搅拌,过滤,洗涤。 |
有红色固体生成,说明粉末中含有 。 |
| 步骤3:将步骤2的滤渣转移到烧杯C中, 。 |
, 说明粉末中含有Fe2O3。(1分) |
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。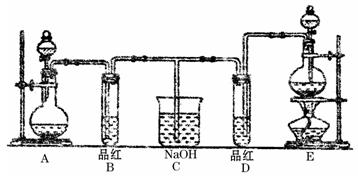
(1)实验室常选用制CO2的发生装置制SO2,实验室用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中装置(填装置序号)制Cl2,通过(填写仪器名称)向烧瓶中加入适量的浓盐酸,反应离子方程式为
。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为
B:,
D:。
(3)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。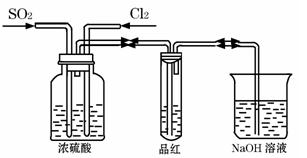
甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是(用化学反应方程式表示):