甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是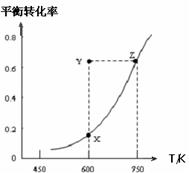
| A.Q>0 |
| B.600K时,Y点甲醇的υ(正) <υ(逆) |
| C.从Y点到Z点可通过增大压强实现 |
| D.从Y点到X点可通过使用催化剂实现 |
与纯水的电离相似,液氨中存在着微弱的电离:
2NH3
 +
+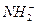
据此判断以下叙述中错误的是( )
A.液氨中含有NH3、 、 、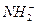 等粒子 等粒子 |
B.一定温度下液氨中C( )·C( )·C(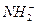 )是一个常数 )是一个常数 |
C.液氨的电离达到平衡时C(NH3)=C( )=C( )=C(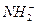 ) ) |
D.只要不加入其他物质,液氨中C( )=C( )=C(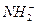 ) ) |
某强酸溶液pH=A,强碱溶液pH=b,已知A+b=12,酸碱溶液混合后pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的正确关系为( )
| A.V(酸)=102V(碱) | B.V(碱)=102V(酸) | C.V(酸)=2V(碱) | D.V(碱)=2V(酸) |
水的电离过程H2O H++OH-,在不同温度下其离子积为KW(25 ℃)=1.0×10-14,KW(35 ℃)=2.1×10-14。则下列叙述正确的是( )
H++OH-,在不同温度下其离子积为KW(25 ℃)=1.0×10-14,KW(35 ℃)=2.1×10-14。则下列叙述正确的是( )
| A.C(H+)随着温度的升高而降低 | B.在35 ℃时,C(H+)>C(OH-) |
| C.水的电离常数K(25 ℃)>K(35 ℃) | D.水的电离是一个吸热过程 |
将pH=1的盐酸加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH升高1,则加入的NaOH溶液的体积为原溶液的()
| A.1/9 | B.1/10 | C.9/11 | D.1/12 |
pH=13的强碱与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比为 …( )
| A.1∶9 | B.9∶1 | C.1∶11 | D.11∶1 |