铁的氧化物可用于脱除煤气中的H2S,有一步反应为:Fe3O4(s)+3H2S(g)+H2(g) 3 FeS(s)+4 H2O(g),其温度与平衡常数的关系如图所示。对此反应原理的理解正确的是
3 FeS(s)+4 H2O(g),其温度与平衡常数的关系如图所示。对此反应原理的理解正确的是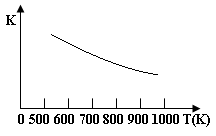
| A.H2S是还原剂 |
| B.脱除H2S的反应是放热反应 |
| C.温度越高H2S的脱除率越大 |
| D.压强越小H2S的脱除率越高 |
化学在自然资源的开发和利用中具有重要的意义,下列对其认识不正确的是 ()
| A.利用化学知识和化学规律,人们可以更好的开发和利用资源 |
| B.利用化学知识和化学规律,人们可以制取更多物质,丰富物质世界 |
| C.人们在开发和利用资源的过程中,对环境造成了污染,化学对此无能为力 |
| D.人们对资源的开发和利用过程中,时刻不能忘记资源的可持续性发展 |
某有机物X,经过下列变化后可在一定条件下得到乙酸乙酯。则有机物X是()
| A.C2H5OH | B.C2H4 | C.CH3CHO | D.CH3COOH |
液晶是一类新型材料:MBBA是一种研究得较多的液晶化合物。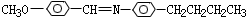 它可以看作是由醛A和胺B去水缩合的产物:
它可以看作是由醛A和胺B去水缩合的产物: 、
、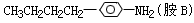 ,醛A的异构体甚多,其中属于酯类化合物,而且结构式中有苯环结构的异构体就有M个;胺B也有多种异构体,其中-C4H9处在对位的苯胺就有N个,则M和N的值分别为 ( )
,醛A的异构体甚多,其中属于酯类化合物,而且结构式中有苯环结构的异构体就有M个;胺B也有多种异构体,其中-C4H9处在对位的苯胺就有N个,则M和N的值分别为 ( )
| A. M=3,N=5 | B. M=6,N=4 | C. N=4,N=2 | D. M=5,N=3 |
在人工合成中掺入放射性14C的用途是()
| A.催化剂 | B.媒介质 | C.组成元素 | D.示踪原子 |
以上所述人工合成的牛胰岛素与天然结晶是同一物质的依据是()
| A.扩散作用 | B.渗透作用 | C.相似相溶作用 | D.物质结构相同 |
由甘氨酸(H2NCH2—COOH)和羟基乙酸(HO-CH2-COOH)组成的混合物发生分子间脱水反应,其中生成物属于两分子间脱水的直链产物有 ( )
| A.5种以上 | B.4种以上 | C.3种以上 | D.2种以上 |