镁条在空气中易被氧化。有一根在空气中放置一段时间的镁条样品,其质量为2.8 g,将该样品放入107.8 g稀硫酸中,两者恰好完全反应,反应过程中测得数据如下:
| 数据记录时间 |
t1 |
t2 |
t3 |
t4 |
| 剩余物质质量/g |
110.52 |
l10.46 |
l10.40 |
110.40 |
请计算(写出计算过程):
(1)反应前后减少的质量是__________g,原因是______________________________。
(2)2.8 g样品中含氧化镁的质量是多少?
(3)稀硫酸中溶质的质量分数是多少?
硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产过程中的一个重要化学反应为SiO2 + 2C 高温Si + 2CO↑。若生产5.6 g硅,计算理论上需要二氧化硅(SiO2)的质量。
足量的盐酸与500克碳酸钙反应,生成二氧化碳的质量是多少?
某化学兴趣活动小组用采集的石灰岩样品进行相关实验。将采集到的样品用水冲洗后晾干,称取20.00g样品平均分成两份,分别与足量相同的稀盐酸反应,测定释放出二氧化碳的质量与反应时间的关系如图14所示。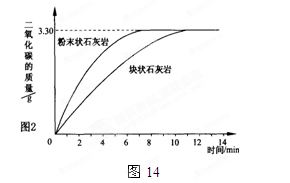
(1)由图中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越,其反应速率越。
(2)求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
食品安全卫生问题牵系千家万户,2008年9月发生的含三聚氰胺的“毒奶粉”事件震惊了全国。三聚氰胺性状为纯白色单斜棱晶体,无味,长期食用含三聚氰胺的食品可致人体的泌尿系统出现结石。因三聚氰胺的含氮量较高,所以被不法分子添加至奶制品中,以“提高”蛋白质含量。三聚氰胺的化学式是C3N6H6,它是由种元素组成的,其中氮元素质量分数为。(精确到0.1%)
“黄铜”是铜锌合金,具有较强机械性能,街头许多“金色”饰品就是用它来制作的。某研究性学习小组为了测定黄铜中铜的质量分数,称取20g黄铜样品,放入烧杯中,然后加入某浓度的稀盐酸100 g(足量),用玻璃棒搅拌至不再产生气泡为止(反应的化学方程式为:Zn+2HCl====ZnCl2+H2 ↑),称量剩余物质的总质量为119.8g。请计算:
⑴实验过程中,产生氢气的质量__,你的计算依据是。
⑵该铜锌合金中铜的质量分数。