一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构如下图:
以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s) + Cu2+(aq) = Zn2+ + Cu(s) △H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
温度相同,浓度均为0.2 mol·L-1的①(NH4)2SO4,②NaNO3,③NH4HSO4,④NH4NO3,⑤CH3COONa溶液,它们的pH由小到大的排列顺序是( )
| A.③①④②⑤ |
| B.①③⑤④② |
| C.③②①⑤④ |
| D.⑤②④①③ |
在由水电离出的c(OH-)=1×10-13 mol·L-1的溶液中,能大量共存的离子组是( )
| A.Fe2+ Na+ N O3- Cl- |
| B.Ba2+ Na+ N O3- Cl- |
| C.S2- S N Na+ |
| D.Mg2+ Na+ Br- ClO- |
室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )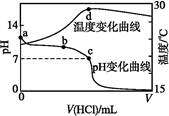
| A.a点由水电离出的c(H+)=1.0×10-14 mol·L-1 |
| B.b点:c( NH4)+c(NH3·H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(N) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
常温下,下列溶液中的微粒浓度关系正确的是( )
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HC)>c(C)>c(H2CO3)
C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(N)>c(OH-)=c(H+)
D.0.2 mol·L-1 CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合:
2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH)
已知NaHSO4在水中的电离方程式为NaHSO4 Na++H++S。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
Na++H++S。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
| A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好呈中性 |
| B.水电离出来的c(H+)=1×10-10 mol·L-1 |
| C.c(H+)=c(OH-)+c(S) |
| D.该温度高于25 ℃ |