工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)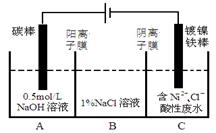
A.碳棒上发生的电极反应:4OH— — 4e— ="=" O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
钠与水反应的现象与钠的下列性质无关的是
| A.钠的熔点较低 | B.钠的密度小于水 |
| C.钠的硬度较小 | D.钠的还原性强 |
NA 表示阿伏加德罗常数,下列说法中正确的是
| A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B.2 g H2所含有的原子数目是NA |
| C.18 g H2O在标准状况下的体积是22.4 L |
| D.在标准状况时,20 mL NH3与60 mL O2所含的分子个数比为2:1 |
下列气体中,对人体无毒害作用的是
| A.Cl2 | B.N2 | C.NH3 | D.SO2 |
下列有关实验安全问题的叙述中,不正确的是
| A.少量的浓硫酸沾到皮肤上,可自行用大量水冲洗 |
| B.取用化学药品时,应特别注意观察药品包装容器上的安全警示标记 |
| C.凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| D.闻任何药品的气味都不能使鼻子凑近药品 |
近来,“PM 2.5”数据监测纳入公众视野。“PM 2.5”是指大气中直径小于或等于2.5微米(1微米=10-6米)的细小颗粒物,也称为可入肺颗粒物。而“PM 2.5”是形成“雾霾”的原因之一。下列有关说法中,正确的是
| A.雾霾没有可能产生丁达尔现象 |
| B.“PM 2.5”没有必要纳入空气质量评价指标 |
| C.雾霾天气不会危害人体健康 |
| D.实施绿化工程,可以有效地防治“PM 2.5”污染 |