根据下列实验操作和现象所得出的结论正确的是
| |
操作 |
现象 |
结论 |
| A |
向某溶液中滴加BaCl2溶液,振荡、静置 |
溶液中出现白色混浊 |
原溶液中一定有SO42- |
| B |
向某溶液中先滴加少量氯水,再滴加KSCN溶液 |
先无明显现象,后溶液变成血红色 |
原溶液中含有Fe2+ |
| C |
将铜片放入浓硝酸中 |
产生大量红棕色气体,溶液变为蓝绿色 |
浓硝酸有强氧化性和酸性 |
| D |
向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀硫酸至红色褪去 |
2 min后,试管里出现凝胶 |
非金属性:S>Si |
我国高速铁路技术世界领先。高速铁路的无缝钢轨是将钢轨间的接头用铝与氧化铁发生铝热反应进行焊接而成的。对于铝热反应:Fe2O3 + 2Al  2Fe + Al2O3,下列说法中正确的是
2Fe + Al2O3,下列说法中正确的是
| A.Fe元素的化合价升高 |
| B.Al被还原 |
| C.Fe2O3发生氧化反应 |
| D.Al是还原剂 |
下列实验装置图所示的实验操作,不能达到相应实验目的的是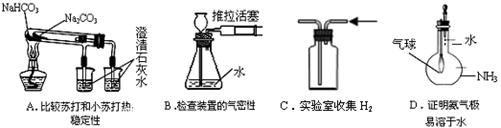
下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 |
| B.用铁粉代替铁钉与稀硫酸反应制取氢气 |
| C.合成氨工业中使用催化剂 |
D.在试管中进 行铝和盐酸反应时,稍微加热 行铝和盐酸反应时,稍微加热 |
下列变化中生成物的总能量大于反应物的总能量的是
| A.H + H = H—H |
| B.H—Cl =" H" + Cl |
C.Mg  + 2HCl = MgCl2 + H2 ↑ + 2HCl = MgCl2 + H2 ↑ |
| D.H2SO4 + 2NaOH = Na2SO4 + 2H2O |
下列各组物质性质的比较中,不正确的是
| A.热稳定性:SiH4<PH3<H2O | B.酸性:H3PO4>H2SO4>HClO4 |
| C.碱性:NaOH > Mg(OH)2> Al(OH)3 | D.金属性:Na > Mg > Al |