[化学一选修2:化学与技术]海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和________池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜 只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用_______(写一点即可)。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。
①海水不能直接通入到阴极室中,理由是______________.
②A口排出的是_______(填“淡水”或“浓水”)。
(3)用苦卤(含 Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:
①若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为___________。
②通过苦卤中通入Cl2已获得含溴的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液________。
③向蒸馏塔中通入水蒸气加热,控制温度在90 左右进行蒸馏的原因是___________。
左右进行蒸馏的原因是___________。
下列关于各实验装置的叙述中不正确的是( )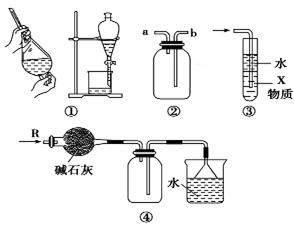
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
已知铜在常温下能被HNO3溶解,反应方程式为:
3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式
___________________________________________________________________
(2)上述反应中,氧化剂是 _____________,氧化产物是_____________。
(3)每2 molCu参加反应,转移的电子__________ 个,在反应的硝酸中没有参加氧化还原反应的硝酸占总硝酸的________________。
(10分)某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均己略去) 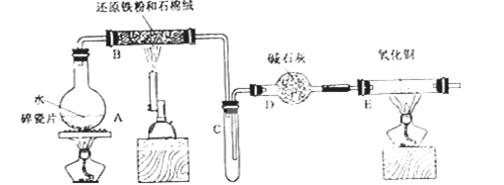
(1)装置B中发生反应的化学方程式是___________________________。
(2)装置E中的现象是________________________________________。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:________________________。
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
滤液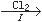 FeCl3溶液
FeCl3溶液 FeCl3·6H2O晶体
FeCl3·6H2O晶体
①步骤Ⅰ中通入Cl2的作用是____________________________________。
②该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明)_______________。
【化学—选修5:有机化学基础】
有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下: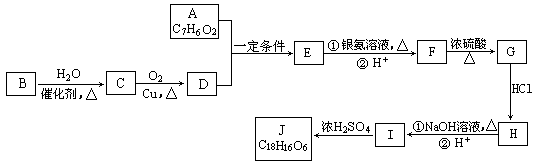
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③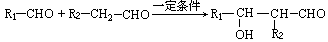
回答以下问题:
(1)A中含有的官能团名称是。
(2)写出有机反应类型B→C,F→G,I→J。
(3)写出F生成G的化学方程式。
(4)写出J的结构简式。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式
。
FeCl3溶液发生显色反应②能发生银镜反应③苯环上只有两个对位取代基④能发生水解反应。
【化学—选修3:物质结构与性质】
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为;
(2)SO42-的空间构型为(用文字描述);中心原子采用的轨道杂化方式是;写出一种与SO42-互为等电子体的分子的化学式:;
(3) 向CuSO4溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是。
(5)CuS比CuO的熔点(填高或低),原因是。
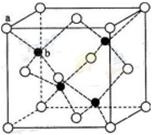
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。