有人分析一些小而可溶的有机分子的样品,发现它们含有碳、氢、氧、氮等元素,这些样品很可能是( )
| A.脂肪酸 | B.氨基酸 | C.葡萄糖 | D.核糖 |
蛋白质是生命的基础物质,下列关于蛋白质的说法正确的是( )
| A.蛋白质的种类很多,它们都能溶解于水 |
| B.蛋白质水解的最终产物是氨基酸 |
| C.蛋白质溶液中加入浓盐酸,颜色变黄 |
| D.蛋白质溶液中加入饱和硫酸铵溶液,蛋白质将变性 |
维生素对人体的作用是( )
| A.构成人体细胞和组织的重要材料 |
| B.能为人体提供能量 |
| C.调节新陈代谢、预防疾病和维持身体健康 |
| D.大量补充人体所需能量 |
医院里检验糖尿病患者的方法是将病人尿液加到CuSO4和NaOH的混合溶液中,加热后若产生红色沉淀,说明病人尿中含有()
| A.脂肪 | B.葡萄糖 | C.乙酸 | D.蛋白质 |
生活中遇到的某些现实问题,常常涉及到化学知识,下列叙述中不正确的是()
12.油脂是油与脂肪的总称,它是多种高级脂肪酸的甘油酯,油脂既是重要食物,又是重要的化工原料,油脂的以下性质和用途与其含有不饱和双键(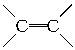 )有关的是()
)有关的是()
| A.适量摄入油脂,有助于人体吸收多种脂溶性维生素和胡萝卜素 |
| B.利用油脂在碱性条件下的水解,可以生产甘油和肥皂(高级脂肪酸钠) |
| C.植物油通过加氢可以制造植物奶油(人造奶油) |
| D.脂肪是有机体组织里储存能量的重要物质 |