根据原子结构及元素周期律的知识,下列推断正确的是
| A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B.核外电子排布相同的微粒化学性质也相同 |
| C.Cl‾、S2‾、Ca2+、K+半径逐渐减小 |
D. 与 与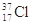 得电子能力相同 得电子能力相同 |
化学与人类生产、生活,社会可持续发展密切相关。下列说法正确的是
| A.蔬菜表面洒少许福尔马林,可保鲜和消毒 |
| B.绿色食品就是不使用化肥农药,不含任何化学物质的食品 |
| C.推广纳米TiO2光触媒技术铺设“生态马路”,将汽车尾气转化为无害物质 |
| D.推广使用煤液化技术可减少二氧化碳温室气体气体的排放 |
下列实验和结论均正确的是
| 选项 |
操作 |
解释或结论 |
| A |
向某溶液中加入NaOH溶液,出现白色沉淀 |
溶液中一定含有Mg2+ |
| B |
在饱和的SO2溶液中通入NO2气体,溶液的pH变小 |
SO2具有还原性 |
| C |
某酸HX稀释100倍后,pH增加2 |
HX是强酸 |
| D |
配制FeSO4溶液时,应加入过量铁粉和稀硫酸 |
溶液中不断产生FeSO4 |
现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡。六种元素的原子半径与原子序数的关系如图所示。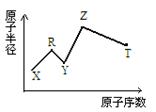
下列推断正确的是
| A.离子半径:Y<Z |
| B.氢化物的沸点和稳定性排序 :R<Y |
| C.最高价氧化物对应的水化物的酸性 :T> R |
| D.由X、R、Y、Z四种元素组成的化合物水溶液一定显酸性 |
在55℃时,下列说法正确的是
| A.向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B.pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
| C.饱和氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO) |
| D.0.1mol/L的(NH4)2SO4溶液中:c(NH4+) > c(SO42-) > c(H+) > c(OH-) |
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
FeCl3溶液能腐蚀Cu |
Fe的金属性强于Cu |
| B |
Na2O2使酚酞溶液变红 |
Na2O2是碱性氧化物 |
| C |
Cl2可部分与水反应 |
用排饱和食盐水法收集Cl2 |
| D |
浓H2SO4可干燥NO和SO2 |
NO和SO2还原性都弱 |