S-诱抗素能保持鲜花盛开,S-诱抗素的分子结构,如图,下列关于该物质说法正确的是
| A.S-诱抗素能发生酯化反应的官能团有2种 |
| B.S-诱抗素含有苯环、羟基、羰基、羧基、碳碳双键 |
| C.1 mol S-诱抗素与足量金属Na反应生成0.5 mol H2 |
| D.该化合物不能发生聚合反应 |
可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应
①Br2 + 2e-= 2Br-②2Br- - 2e-= Br2③Zn – 2e-= Zn2+④Zn2+ + 2e-= Zn其中表示充电时的阳极反应和放电时的负极反应的分别是
| A.②和③ | B.②和① | C.③和① | D.④和① |
电解饱和食盐水,当阴极附近有0.4 mol NaOH生成时,阳极放出
| A.0.2 mol H2 | B.0.2 mol Cl2 |
| C.O.4 mol H2 | D.0.4 mol Cl2 |
1g H2完全燃烧生成液态水放出a KJ的热量,下列热化学方程式正确的是
| A.H2(g)+ 1/2 02(g)= H2O(l)△H =-aKJ.mol-1 |
| B.2H2(g) + O2(g) = 2H2O(l)△H =-4aKJ.mol-1 |
| C.2H2(g) + O2(g) = 2H2O(l)△H =+4aKJ.mol-1 |
| D.H2(g) + 1/2 O2(g) = H2O(g) △H =-2aKJ.mol-1 |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是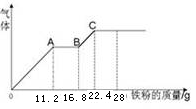
| A.原混合液中NO3-的物质的量为0.4mol |
| B.OA段产生是NO,AB段反应为2Fe3++Fe = 3Fe2+,BC段产生氢气 |
| C.溶液中最终溶质为FeSO4 |
| D.c(H2SO4)为5mol·L-1 |
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C