现有下列仪器或用品:①铁架台(含铁圈、各种铁夹);②锥形瓶;③滴定管(酸式与碱式);④烧杯(若干个);⑤玻璃棒;⑥天平(含砝码);⑦滤纸;⑧量筒;⑨漏斗。有下列药品:①NaOH固体;②0.1000mol/L的标准NaOH溶液;③未知浓度的盐酸;④Na2CO3溶液。试回答以下问题。
(1)做酸碱中和滴定时,还缺少的试剂是 。
(2)小明在做“研究温度对反应速率的影响”实验时,他往两支试管均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中, B试管置于冷水中,记录溶液褪色所需的时间。褪色所需时间tA tB(填“>”、“=”或“<”)。
写出该反应的离子方程式 。
(3)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000 mol·L-1 KMnO4溶液装入 (填“酸式”或“碱式”)滴定管,进行滴定操作。
在实验中发现,刚滴下少量KMnO4溶液时,溶液紫红色并没有马上退去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪色了,可能原因是 ;
当 ,说明达到滴定终点。
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4溶液的平均体积为 mL,此样品的纯度为 。(已知H2C2O4的相对分子质量为90)
| 序号 |
滴定前读数 |
滴定后读数 |
| 1 |
0.00 |
20.01 |
| 2 |
1.00 |
20.99 |
| 3 |
0.00 |
21.10 |
④误差分析:下列操作会导致测定结果偏高的是 。
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
根据下式所示的氧化还原反应设计一个原电池:
(1)装置可采用烧杯和盐桥,画出此原电池的装置简图。
①注明原电池的正极和负极;
②注明外电路中电子的流向。
(2)写出两个电极上的电极反应。
)X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物具有相同的电子数,一般情况下X的单质只有氧化性。
(1)写出实验室制取W2反应的离子方程式 。
(2)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究YX2和W2的性质。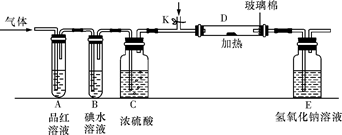
①分别通入YX2和W2,在装置A中观察到的现象是否相同(填“相同”或“不相同”) ;若装置D中装的是铁粉,当通入W2时D中观察到的现象为 ;若装置D中装的是五氧化二钒,当通入YX2时,打开K通入适量X2,化学反应方程式为 ;
②若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,则该反应的化学方程式为 。
(3)某同学将足量的YX2通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加入过量(填字母) ,可以看到白色沉淀生成。
| A.氨水 | B.稀盐酸 |
| C.稀硝酸 | D.氯化钙 |
(4)若由元素Y和X组成-2价酸根Z,Z中Y和X的质量比为Y∶X=4∶3,当W2与含Z的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出W2与Z的溶液完全反应产生浅黄色沉淀的离子方程式
(1)下面A~F是中学化学实验中常见的几种仪器:
A.坩埚 B.容量瓶 C.试管 D.托盘天平 E.玻璃棒
① 其中仪器上标示出仪器的使用温度的 __________(填写编号);
②称取 10.5 g固体样品(1 g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为____ g.
(2)若要配制500mL 1mol/L NaOH溶液时,下列哪些操作会使实验结果偏高的是,偏低,无影响。(填写编号)
A.定容,振荡,摇匀溶液后,发现液面低于刻度线,再补加水
B.称量时,固体放在右盘,砝码放在左盘(未使用游码)
C.原容量瓶洗涤后未干燥
D.定容时俯视刻度线
E.移液时,未洗涤烧杯和玻璃棒
F.在烧杯中溶解NaOH固体后,未冷却立即将溶液注入容量瓶中
2005年的诺贝尔化学奖颁给了3位在烯烃复分解反应研究方面做出突出贡献的化学家。烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——丁烯和乙烯。
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。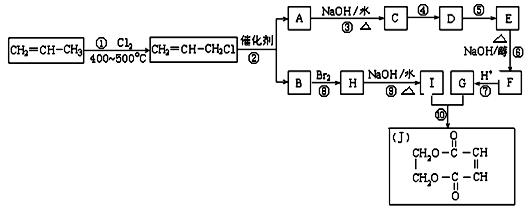
请按要求填空:
(1) 写出下列反应的反应类型:
①______________,⑥______________,⑧______________。
(2) 反应②的化学方程式是___________________________________________。
(3) 反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是_____________________________________________,
物质E的结构简式是_______________________。
(4) 反应⑩的化学方程式是___________________________________________。
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH 与Cl2反应生成的是KClO3。写出在温度较高时KOH 与Cl2反应的化学方程式
,当反应中转移5 mol电子时,消耗的氯气是mol。
(2)在反应液I中加入KOH固体的目的是(填编号)。
| A.与反应液I中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供碱性的环境 |
| D.使KClO3转化为 KClO |
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为。
(4)如何判断K2FeO4晶体已经洗涤干净。