下列图示与对应的叙述不相符的是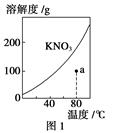


| A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液 |
| B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C.图3表示0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸溶液得到的滴定曲线 |
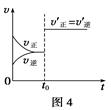
| D.图4表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是增大压强 |
下列各组离子在溶液中能大量共存的是( )
| A.Na+、Al3+、Cl-、SO42- | B.Cu2+、Cl-、NO3-、OH- |
| C.H+、Na+、CO32-、NO3- | D.H+、SO42-、NO3-、OH- |
下列离子方程式书写正确的是()
| A.Cl2和澄清石灰水反应:Cl2+2OH-=Cl-+ClO-+H2O |
| B.NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO2↑+H2O |
| C.向AlCl3溶液中加入过量的氨水:A13++3OH-=Al(OH)3↓ |
| D.实验室用大理石和稀醋酸制取CO2:CaCO3+2H+=Ca2++CO2↑+H2O |
用NaCl固体配制0.1mol/L的NaCl溶液,下列操作或说法正确的是()
| A.将5.85gNaCl固体溶于1L水中可配成0.1mol/L的NaCl溶液 |
| B.称量时,将固体NaCl直接放在天平左盘上 |
| C.固体溶解后,将溶液转移到容最瓶中,然后向容最瓶中直接加水稀释到刻度线 |
| D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果 |
NA代表阿伏加德罗常数,下列有关NA的叙述中正确的是()
| A.1mol任何物质所含的微粒数均为NA |
| B.14g氮气所含的N 原子数为NA |
| C.标准状况下22.4L水所含的H2O分子数为NA |
| D.在钠与氧气的反应中,lmol钠失去电子的数目为2NA |
标准状况下①6.72LCH4②3.01×1023个HCl分子 ③13.6gH2S ④0.2molNH3,下列对这四种气体的关系从大到小表达不正确的是()
| A.体积②>③>①>④ | B.密度②>③>④>① |
| C.质量②>③>①>④ | D.氢原子个数①>④>③>② |