常温下,H3PO4与NaOH溶液反应的体系中,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示[已知Ca3(PO4)2难溶于水]。下列有关说法不正确的是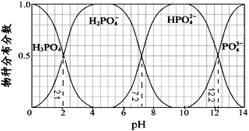
| A.H3PO4的Ka3=10–12.2,HPO42–的水解平衡常数为10–6.8 |
| B.Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性 |
| C.pH=13时,溶液中各微粒浓度大小关系为:c(Na+)>c(HPO42–)>c(PO43-)>c(OH-)>c(H+) |
| D.为获得尽可能纯的NaH2PO4,pH应控制在4~5.5左右 |
配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高()
| A.所用NaOH已经潮解 | B.向容量瓶中加水未到刻度线 |
| C.有少量NaOH溶液残留在烧杯里 | D.称量时误用“左码右物” |
下列有关物质的性质和该性质的应用均正确的是()
| A.常温下浓硫酸是铝发生钝化,可在常温下用铝制贮藏贮运浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.氯气具有还原性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
某固体物质只含有钠和氧两种元素,将它放在足量的水中产生两种气体,这两种气体又可以在一定条件下反应生成水。则原固体物质的组成是()
| A.Na2O2与Na2O | B.Na和NaOH | C.Na2O2和Na | D.Na和Na2O |
按照物质的树状分类和交叉分类,HNO3应属于:①酸②氢化物③氧化物④含氧酸⑤一元酸⑥强酸⑦化合物⑧有机物⑨无机化合物
| A.①④⑤⑥⑦⑨ | B.①②③④⑤⑥⑦⑨ | C.①②④⑧ | D.①④⑤⑥ |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是()
| A.60 mL | B.45 mL | C.30 mL | D.15 mL |