右图是一种正在投入生产的大型蓄电系统的原理图。电池的中间为只允许钠离子通过的离子选择性膜。电池充、放电的总反应方程式为:2Na2S2+NaBr3 Na2S4+3NaBr
Na2S4+3NaBr
下述关于此电池说法正确的是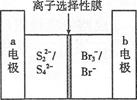
| A.充电的过程中当O.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 |
| B.电池放电时,负极反应为:3NaBr一2e-=NaBr3+2Na |
| C.充电过程中,电极a与电源的正极相连 |
| D.放电过程中钠离子从右到左通过离子交换膜 |
与OH具有相同质子数和电子数的粒子是()
| A.H2O | B.F- | C.Na+ | D.NH3 |
制取氯乙烷(CH3一CH2Cl)的最好的方法是()
| A.乙烷与氯气发生取代反应 | B.乙烯与氯气发生加成反应 |
| C.甲烷与氯气发生取代反应 | D.乙烯与氯化氢发生加成反应 |
下列物质完全燃烧时,生成的二氧化碳的物质的量与生成水的物质的量相同的是()
| A.CH4 | B.C2H6 | C.C3 H6 H6 |
D.C6H6 |
下列物质中,属于含有共价键的离子化合物的是()
| A.KOH | B.Br2 | C.MgCl2 | D.H2S |
下列各组性质的比较中,不正确的是()
| A.碱性:NaOH>Mg(OH)2 | B.热稳定性:NH3>PH3 |
| C.失电子能力:K>Na | D.原子半径:CI>S |