下列有关化学反应,对其反应类型的判断,正确的是()
①
②
③
④
| A. | ①分解反应 | B. | ②置换反应 | C. | ③复分解反应 | D. | ④化合反应 |
有机物在日常生活中应用广泛,下列说法正确的是()
| A. | 甲烷是沼气的主要成分,沼气是可再生的生物能源 |
| B. | 工业酒精的主要成分是甲醇,甲醇饮后会使人失明,甚至死亡.因此,工业酒精是禁止用来配制饮用酒的 |
| C. | 乙酸俗称醋酸,是食醋的主要成分,纯乙酸是无色、有强烈刺激性气味的液体,且无腐蚀性,可直接食用 |
| D. | 合成材料主要包括塑料、橡胶和合成纤维 |
科学研究中常用图象来表示两个量(
)之间的关系,以使研究的间压变得直观明了.在某温度下.将少量氧化钙加入到一定量的饱和氢氧化钙溶液中.图甲表示整个过程中温度的变化,图乙表示氢氧化钙的溶解度与温度的关系.小阳同学要挟据观察和思考,作出了如图丙所示的图象,此图象反映了该过程中()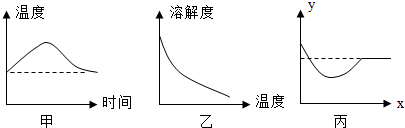
| A. | 溶质的质量与时间的关系 |
| B. | 溶剂的质量与时间的关系 |
| C. | 溶质的溶解度与时间的关系 |
| D. | 溶质的质量分数与时间的关系 |
某校实验室将药品分类后放在不同的药品柜里,巳存放的部分药品如下:
| 药品柜编号 |
① |
② |
③ |
④ |
… |
| 药品 |
氢氧化钠 氢氧化钙 |
盐酸 硫酸 |
二氧化锰氯化铜 |
氯化钠 硫酸钠 |
… |
该实验室新购进部分生石灰和纯减.应将它们分别放在()
| A. |
③和① |
B. |
④和① |
C. |
③和④ |
D. |
①和② |
下列除去杂质的方法,错误的是()
| A. | 除去 中的少最水蒸气:通过浓硫酸 |
| B. | 除去 中的少最 :通入足量的 溶液,干操 |
| C. | 除去 溶液中少量的 :加入适量 溶液,过滤 |
| D. | 除去 溶液中少量的 :加入足量的铁屑充分反应后,过滤 |
正确的操作是实脸成功的基础.下列几项实验操作正确的是()
| A. |
用火柴点燃酒精灯 |
B. |
量筒读数 |
C. |
滴加溶液 |
D. |
洋葱表皮细胞装片制作 |