向AgNO3溶液中加入过量氨水,可生成[Ag(NH3)2]OH。下列说法正确的是
| A.氨气极易溶于水,所得的氨水中存在3种不同的氢键 |
| B.[Ag(NH3)2]+中含有6个σ键 |
| C.[Ag(NH3)2]OH所含有的化学键有离子键、极性共价键和配位键 |
| D.在[Ag(NH3)2]+离子中Ag+给出孤对电子,NH3提供空轨道 |
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:
X(g)+2Y(g) 2Z(g)
2Z(g)
此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内各物质的浓度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1∶2∶2 |
| D.单位时间消耗0.1 mol X同时生成0.2 mol Z |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是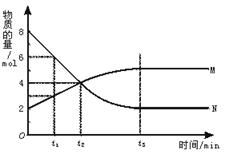
| A.反应的化学方程式为:2M===N |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
在5 L的密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g) 2C(g),达平衡时,在相同温度下测得容器内混合气体的压强是反应前的
2C(g),达平衡时,在相同温度下测得容器内混合气体的压强是反应前的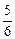 ,则A的转化率为
,则A的转化率为
| A.67% | B.50% | C.25% | D.5% |
在一定温度下,可逆反应X(g)+3Y(g) 2Z(g)达到平衡的标志是
2Z(g)达到平衡的标志是
| A.Z的生成速率与Z的分解速率相等 |
| B.单位时间生成a mol X,同时生成3a mol Y |
| C.X、Y、Z的浓度不再变化 |
| D.X、Y、Z的分子数比为1∶3∶2 |
在一密闭容器中,反应a A(g) b B(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
b B(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
| A.平衡向正反应方向移动了 |
| B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 |
| D.a>b |