短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是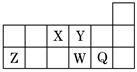
| A.元素的非金属性:Y>W |
| B.阴离子的还原性:W2->Q- |
| C.离子半径:Y2->Z3+ |
| D.Q、W、Y对应的氢化物的沸点逐渐降低 |
将两种气态烃组成的混合气体0.1mol,完全燃烧后得到0.16mol二氧化碳和3.6克水, 则混合气体中 ( )
| A.混合气体中一定有甲烷 | B.混合气体中一定有甲烷和乙烯 |
| C.混合气体中一定有乙烷 | D.混合气体中一定有乙炔 |
下列关于蛋白质的叙述错误的是( )
| A.蛋白质是组成细胞的基础物质,蛋白质是一种纯净物 |
| B.天然蛋白质水解的最终产物都是α—氨基酸 |
| C.大多数酶是具有催化作用的蛋白质,其催化特点是不需加热、专一性、高效性 |
| D.高温灭菌消毒的原理是加热后蛋白质变性,从而细菌死亡 |
某有机物结构简式为 ,下列对其化学性质的判断中不正确的是( )
,下列对其化学性质的判断中不正确的是( )
| A.能被银氨溶液氧化 |
| B.1 mol该有机物只能与1 mol Br2发生加成反应 |
| C.能使KMnO4酸性溶液褪色 |
| D.1 mol该有机物只能与1 mol H2发生加成反应 |
用括号内的试剂和方法,除去下列各物质中所含有的少量杂质,其中正确的是( )
A 苯中少量苯酚(NaOH溶液,分液)
B 乙烷中少量乙烯(H2,催化剂加热)
C 乙酸乙酯中少量乙醇(NaOH溶液,分液)
D 乙烯中少量SO2(溴水,洗气)
属于天然高分子化合物的是( )
①牛油②棉麻③塑料④蚕丝⑤酚醛树脂⑥锦纶
| A.①⑤⑥ | B.①②④ | C.⑤⑥ | D.②④ |