下列溶液中各微粒的浓度关系不正确的是
| A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+ c(CH3COOH)=0.1mol/L |
| B.NaHCO3溶液中: c(OH-) = c(H+) + c(H2CO3)-c(CO32-) |
| C.CH3COONa溶液中:c(Na+)> c(CH3COO-)> c(OH-)> c(H+) |
| D.Na2S溶液中:2 c(Na+)= c(S2-) + c(HS-)+ c(H2S) |
化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是()
| A.福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同 |
| B.大量燃烧化石燃料排放的废气中含大量CO2、SO2造成大气污染,从而使雨水pH=5.6形成酸雨 |
| C.以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| D.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
过氧化氢俗称双氧水,它易分解为水和氧气,常作氧化剂、漂白剂和消毒剂,为贮存、运输、使用的方便,工业常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是 ()
| A.MnO2 | B.稀盐酸 | C. Na2CO3 | D.H2S |
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子可能是
| A.Mg2+、Al3+、Fe3+ |
| B.Na+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ |
| D.H+、Mg2+、Al3+ |
有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是
途径① S H2SO4
H2SO4
途径② S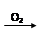 SO2
SO2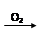 SO3
SO3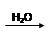 H2SO4
H2SO4
| A.途径①反应中体现了浓HNO3的强氧化性和酸性 |
| B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本 |
| C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- |
| D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高 |
下列物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸②AlCl3溶液与NaOH溶液 ③ 碳酸钠溶液与稀盐酸 ④铁与氯气
| A.全部都是 | B.①②③ | C.②③ | D.③④ |