X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
| B.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| C.元素X不能与元素Y形成化合物X2Y2 |
| D.元素W、R的最高价氧化物的水化物都是强酸 |
下列离子方程式与所述事实相符且正确的是()
A.漂白粉溶液在空气中失效: +CO2+H2O=HClO+ +CO2+H2O=HClO+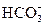 |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-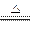 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+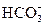 |
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3 +2Fe(OH)3=2 +2Fe(OH)3=2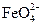 +3 +3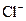 +H2O+4H+ +H2O+4H+ |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH值(不考虑二氧化碳的溶解)。则电解过程中共转移的电子数为()
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |
据报道2008年11月9日德国科学家利用数亿个镍原子(28Ni)对数亿个(82Pb)连续轰击数天后制得一种新原子110X(暂用X表示),它属于一种新元素—第110号元素。这种新元素是有史以来制得最重的元素,存在时间不到千分之一秒。经推知它属于过渡元素。下列关于该元素的叙述中正确的是()
| A.这种原子(110X)的中子数为110 | B.这种元素肯定是金属元素 |
| C.这种元素与铅属同一族 | D.这种元素为第六周期元素 |
下列有关物质结构中的说法正确的是()
| A.78g Na2O2晶体中所含阴阳离子个数均为4NA |
| B.1.5g CH3+中含有的电子数为NA |
| C.3.4g氨气中含有0.6NA个N—H键 |
| D.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
常温常压下,某容器真空时质量为201.0g,当它盛满甲烷时质量为203.4g,而盛满某气体的质量为205.5g,则某气体可能是
| A.氧气 | B.氮气 | C.甲烷 | D.一氧化氮 |