(12分)推断下列化合物的化学式:
(1)X、Y两元素能形成XY2型化合物,XY2中共有38个电子,若XY2是离子化合物,其化学式是__________;若XY2是共价化合物,其化学式是__________。
(2)第三周期内,X、Y两元素的原子序数之差为4,它们组成的XY型化合物,其化学式为____。
(3)1 mol某共价化合物,含有三种短周期元素的原子各1 mol,且三种元素分别属于不同的周期,其质子总数为26 mol,其中一种元素的最外层有7个电子,则该物质的化学式为__________。
(4)某非金属X的最低负价为-2,它的最高价氧化物对应的水化物为强酸,则这种酸的化学式是__________。
(5)X元素的最高正价和负价绝对值之差为6,Y元素的化合价为+1,Y元素和X元素原子的次外电子层上都有8个电子,X和Y形成的化合物在水溶液中能电离出电子层结构相同的离子,则该化合物是__________。
某一种氯化钠与氯化钾的混合物,它所含钾原子和钠原子的物质的量之比为3:1,求:(1)混合物中氯化钾的质量分数?(2)含1 mol氯原子的该混合物的质量?
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,可证明滤液中含Na+,不含K+。
由上述现象推断:
(1)该混合物中一定含有 ;一定不含有,可能含有。
(2)如要检验其是否存在,将如何操作。
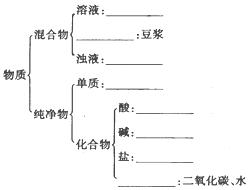
现有下列物质:
| A.豆浆, | B.食盐水, | C.铁, | D.硫酸,E.氢氧化钠固体,F.纯碱,G.泥水,H.二氧化碳,I.水。请将它们的序号或所属类别填充到下列横线上 |
CO和CO2的混合气体18 g,完全燃烧后测得CO2体积为11.2 L(标准状况),
(1)混合气体中CO的质量是 g
(2)混合气体中CO2在标准状况下的体积是 L;
(3)混合气体在标准状况下的密度是 g·L-1。
0.5 mol臭氧(O3)中含有O3的分子数目是,含有O的原子数目是